
【题目】龙葵醛是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。其合成路线如图所示(部分反应产物和反应条件已略去)。

回答下列问题:
(1)X的名称是_______
(2)下列有关龙葵醛和C3H6(烯烃)的说法正确的是________(填序号)。
A.它们的实验式相同 B.它们都能使溴水褪色
C.它们都能发生加成反应 D.它们都含有碳碳双键
(3)反应⑤的试剂和条件是________,反应③的反应类型是__________。
(4)有机物T所含官能团的名称是________,反应④的化学方程式为__________。
(5)在T的同分异构体中,遇氯化铁溶液发生显色反应的有_____种,其中,在核磁共振氢谱上有4 组峰且峰的面积之比为1:2 :3 :6 的结构简式为_________(写出其中的一种)。
(6) 参照上述流程图(如R![]() X……),以2-甲基-1,3-丁二烯为原料,经三步制备2-甲基-1,4-丁二醛,设计合成路线:________________。
X……),以2-甲基-1,3-丁二烯为原料,经三步制备2-甲基-1,4-丁二醛,设计合成路线:________________。
【答案】 异丙苯(或2-苯基丙烷) BC 氢氧化钠溶液、加热 消去反应 羟基 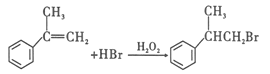 22
22 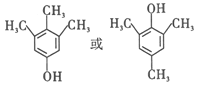

【解析】根据题中各物质转化关系,比较苯和X的分子式以及其它各物质的分子式可知,反应①为加成反应,X在光照条件下发生侧链上取代生成Y,Y发生消去反应生成Z,Z与溴化氢发生加成反应生成W,W在碱性条件下加热,发生水解反应生成T,T发生氧化反应生成龙葵醛,根据龙葵醛的结构可反推T得为![]() ,W为
,W为![]() ,Z为
,Z为![]() ,Y为
,Y为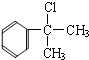 或
或![]() ,X为
,X为![]() ;
;
(1)X为![]() ,名称为异丙苯(或2-苯基丙烷) ;
,名称为异丙苯(或2-苯基丙烷) ;
(2)根据龙葵醛的分子式C9H10O,结构中含有官能团醛基,烯烃C3H6中含有官能团碳碳双键,进行如下判断:.它们的实验式不相同 ,A 错误;醛基被溴水氧化为羧基,溴水褪色,碳碳双键与溴发生加成,溴水褪色,B正确;醛基、碳碳双键都能与氢气发生加成,C正确;苯环无双键,醛基含碳氧双键,D错误;正确答案选BC;
(3)根据转化流程看出,W 为溴代烃,T为醇,溴代烃在氢氧化钠的水溶液中加热发生取代反应生成相应的醇,正确答案:氢氧化钠溶液、加热; 从流程看出,由Y为氯代烃 变为含氧衍生物,减少了HCl,该反应为消去反应,正确答案:消去反应;
(4)有机物T为醇,所含官能团的名称是羟基;由Z变为W,发生加成反应,溴原子应该加不饱和碳原子的端位碳上,这样才能被氧化为醛基;正确答案为: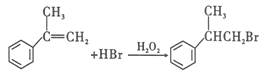 ;
;
(5)在T(C9H12O)的同分异构体中,遇氯化铁溶液发生显色反应,该有机物的结构中必须含有酚羟基,这样环上有一个3个碳的取代基,环上有一个乙基和一个甲基2个取代基,环上有3个甲基取代基,和羟基位置吸相比,有邻间对三种位置,这样的结构共有22种;从上述22种中挑选出符合核磁共振氢谱上有4 组峰且峰的面积之比为1:2 :3 :6 的有机物,任写一个;正确答案:22;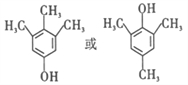
(6) 醇要氧化为醛,醇中的羟基必须连在主碳链的端位碳上,而对于2-甲基-1,3-丁二烯来说,只有发生1,4加成,溴原子才能加成在两端的不饱和碳上,而要实现这样的变化,必须满足双氧水作为反应条件才能实现。综上,正确答案:
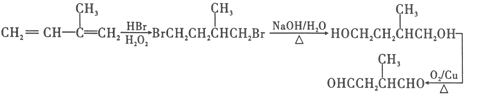 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】碳酸钠的结晶水合物在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体( Na 2CO3·nH2O )。为测定其组成,某同学在不同温度下加热样品(温度逐渐升高),实验结果记录如 下:
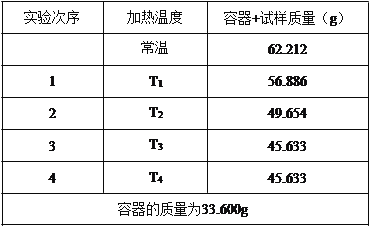
(1)该实验称量用的仪器是_____;实验记录中的容器是指_____(填仪器名字);冷却必须放在_____中进行(填仪器名称)。
(2)该学生停止实验的依据是_____。
(3)该样品中 n 的值为_____。(保留一位小数)
(4)若该实验过程中出现下列操作,其中可能会使实验结果 n的值偏大的是(______)
A.容器内壁原来附着有受热不分解的物质
B.碳酸钠晶体样品已有少量风化
C.加热后容器在空气中冷却
D.加热过程中有少量晶体溅出
(5)如果碳酸钠晶体样品不纯,测定结果(______)
A.没有偏差 B.一定偏小
C.一定偏大 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A.使用催化剂 B.适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)下图能正确表示该反应中能量变化的是________。
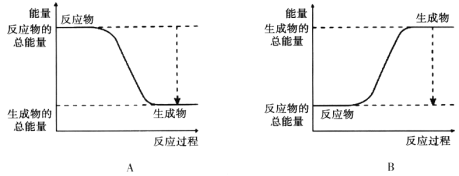
(3)从断键和成键的角度分析上述反应中能量的变化。
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
请填写下表:
化学键 | 填“吸收热量”或“放出热量” | 能量变化(kJ) | |
拆开化学键 | 2molH2化学键 | ________ | ________ |
1molO2化学键 | |||
形成化学键 | 4molH-O键 | ________ | ________ |
总能量变化 | ________ | ________ | |
(4)氢氧燃料电池的总反应方程式为2H2 +O2=2H2O。其中,氢气在______极发生_______反应。电路中每转移0.2mol电子,标准状况下消耗H2的体积是______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下有H2RO4=H++HRO4-、HRO4-![]() H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是
H++RO42-,现有物质的量浓度都为0.1mol/L的三种溶液:①NaHRO4溶液; ②H2RO4溶液; ③Na2RO4溶液。下列说法正确的是
A. ②和③等体积混合后的溶液中: c( Na+)= c( HRO4-)+c(H2RO4) +c(RO42-)
B. 100mL①溶液中: n(HRO4-)+n(RO42-)+n(OH-)-n(H+)= 0.01
C. ①和②等体积混合后的溶液中可能的离子浓度为c( HRO4-)>c(H+)>c(Na+)
D. 若①和③等体积混合后,会抑制水的电离,则HRO4-的电离程度肯定大于RO42-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将钠投入到滴有无色酚酞溶液的水中,下列有关叙述中错误的是( )
A.Na浮在水面上
B.有气体产生
C.水溶液变为蓝色
D.Na熔化成小球并在水面上四处游动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是( )
A.钠的化合物
B.可与硝酸反应
C.可溶于水
D.电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A.950 mL,111.2 g
B.500 mL,117 g
C.1 000 mL,117 g
D.任意规格,111.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,还含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
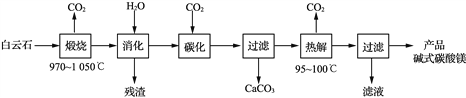
(1) “煅烧”时发生主要反应的化学方程式为____________________________。
(2)常温常压下“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
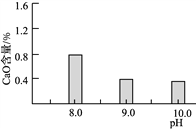
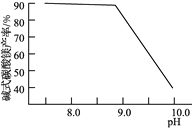
图1 CaO含量与碳化终点pH的关系 图2 碱式碳酸镁产率与碳化终点pH的关系
①应控制“碳化”终点pH约为________,发生的主要反应的化学方程式为______________________和____________________。
②图2中,当pH=10.0时,镁元素的主要存在形式是____________(写化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为________________________________。
(4)该工艺为达到清洁生产,可以循环利用的物质是____________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置完成对应的实验,能达到实验目的的是
A. 制取并收集少量氨气 
B. 比较NaHCO3和Na2CO3的热稳定性
C. 制取并检验乙烯
D. 比较盐酸、碳酸、硅酸的酸性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com