
| A. | pH=2的硫酸 | B. | 0.01mol/L的硝酸 | C. | 0.01mol/L的甲酸 | D. | pH=2的醋酸 |
分析 常温下pH=12的NaOH溶液浓度为0.01mol/L,NaOH和酸等体积混合后,再滴入几滴石蕊试液,溶液呈红色,溶液呈酸性,说明酸有剩余,据此分析解答.
解答 解:常温下pH=12的NaOH溶液浓度为0.01mol/L,
A.pH=2的硫酸中c(H+)=0.01mol/L,硫酸中c(H+)等于NaOH溶液中c(OH-),等体积混合时,二者恰好反应生成强酸强碱盐,溶液呈中性,故A错误;
B.等浓度、等体积的硝酸和NaOH恰好反应生成硝酸钠,硝酸钠为强酸强碱盐,其溶液呈中性,故B错误;
C.等浓度、等体积的甲酸和NaOH恰好反应生成甲酸钠,甲酸钠为强碱弱酸盐,其溶液呈碱性,故C错误;
D.pH=2的醋酸浓度大于0.01mol/L,等体积混合时醋酸有剩余,溶液呈酸性,故D正确;
故选D.
点评 本题考查酸碱混合溶液定性判断,同时考查学生分析问题、解决问题能力,正确判断混合溶液中的溶质及其性质是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )| A. | O点溶液中所含溶质的化学式为NaOH、Na2CO3 | |
| B. | 常温下,a点溶液显碱性 | |
| C. | 标准状况下,通入CO2的体积为4.48L | |
| D. | 原NaOH溶液的物质的量浓度为2.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使含NH4+的溶液放出NH3的溶液:Na+、Mg2+、SO42-、Cl- | |
| B. | 1.0mol•L-1的NaNO3的溶液:H+、Cu2+、I-、SO42- | |
| C. | $\frac{{K}_{W}}{c({OH}^{-})}$=0.001mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| D. | FeCl3溶液:NH4+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
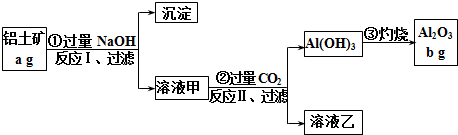
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
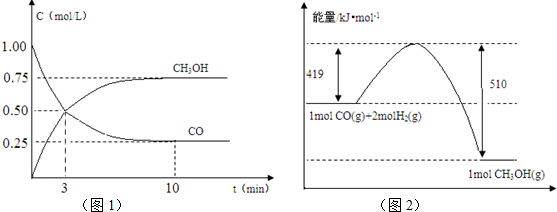
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
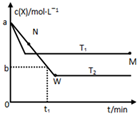 恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )
恒容密闭容器中发生反应:2X(g)?Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图.下列叙述正确的是( )| A. | M点的正反应速率v正大于N点的逆反应速率v逆 | |
| B. | T2下,在0~t1时间内v(Y)=$\frac{(a-b)}{t_1}$(mol•L-1•min-1) | |
| C. | 该反应进行到M点放出的热量大于进行到W点放出的热量 | |
| D. | M点时再加入一定量X,平衡后X的转化率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮的固定包括人工固氮和自然固氮 | B. | 工业合成氨属于人工固氮 | ||
| C. | 自然固氮中氮元素被氧化 | D. | 氮的固定中参与元素至少有两种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeCl2、NaI的混合溶液中加入硫氰化钾溶液,再滴加少量氯水,溶液没有变为红色,说明还原性:Fe2+<I- | |
| B. | 检验AlNH4(SO4)2溶液中的NH4+:取样于试管中,向溶液中加入少量NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体 | |
| C. | 检验Na2SO3和Na2SO4的混合溶液中的SO42-:先加足量稀硝酸,再加氯化钡溶液 | |
| D. | 验证碳酸钠溶液显碱性是CO32-导致的:先加酚酞试液,溶液变红,再加硫酸溶液,红色褪去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com