
 ,该分子中共平面的原子最多有( )
,该分子中共平面的原子最多有( )| A. | 20个 | B. | 18个 | C. | 22个 | D. | 24个 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:推断题
醛在有机合成中十分重要,已知如下反应:

由枯茗醛合成兔耳草醛 的传统合成路线如图所示:
的传统合成路线如图所示:

(1)写出试剂X的结构简式:__________________。
(2)写出有机物B的结构简式:__________________________。
(3)写出有机物C →兔耳草醛的化学方程式:________________________。
(4)人们最新研究的兔耳草醛的合成路线,该路线原子利用率理论上可达100%:

试写出D的结构简式:_________________________。
(5)芳香族化合物Y与枯茗醛互为同分异构体,Y具有如下特征:
a.不能发生银镜反应,可发生消去反应;
b.核磁共振氢谱显示:Y消去反应产物的环上只存在一种化学环境的氢原子。写出Y所有可能的结构简式:____________________________。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5 mL0.2 mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生 气体,最后沉淀逐渐减少至消失。
气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43 g。
下列说法中正确的是:( )
A.该溶液中一定不含 Ba2+ 、Mg2+、A13+、SiO32-、Cl-
Ba2+ 、Mg2+、A13+、SiO32-、Cl-
B.该溶液中一定含有K+、AlO2-、CO32-、Cl-
C.该溶液是否有K+ 需做焰色反应(透过蓝色钴玻璃片)
D.可能含有Cl-
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:选择题
常温下,将一定量的氯气通入100mL 4mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.充分反应后,下列说法正确的是(NA为阿伏加德罗常数)( )
A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA
B.当溶液中Na+为0.4 NA时,溶液中的Cl﹣为0.2 NA
C.当电子转移数目为0.2 NA时,溶液质量增加7.1 g
D.当溶液质量增加7.1 g时,溶液中ClO﹣约为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
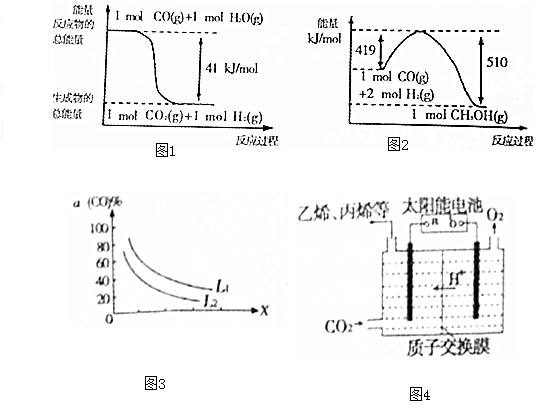
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.46 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
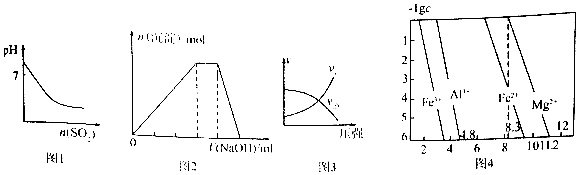
| A. | 图1表示常温下,将SO2气体通入溴水中,所得溶液pH的变化 | |
| B. | 图2表示向NH4A1(SO4)2溶液中逐滴滴入NaOH溶液,沉淀总物质的量(n)随NaOH溶液体积(V)的变化 | |
| C. | 图3表示T°C时,对于可逆反应:A(g)+B(g)?2C(g)+D(g)△H>0,正、逆反应速率与压强的关系 | |
| D. | 图4表示常温下,几种难溶氢氧化物的饱和溶液中金属离子浓度的负对数与溶液PH的关系,则在pH=7的溶液中,Fe3+、A13+、Fe2+能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝热反应 | ||
| C. | 铝与稀盐酸 | D. | 灼热的炭与CO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏伽德罗常数就是 6.02×1023 mol-1 | |
| B. | 1mol任何粒子的粒子数叫做阿伏伽德罗常数 | |
| C. | 1molNaOH溶于1L水中得到 1.0 mol/L的 NaOH溶液 | |
| D. | 0.012Kg碳中含有的碳原子数就叫做阿伏伽德罗常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com