
【题目】在相同的条件下(500 ℃),有相同体积的甲、乙两容器,甲容器充入1 g O2和1 g SO2,乙容器充入2 g O2和2 g SO2。下列叙述中错误的是( )
A. 化学反应速率:乙>甲
B. 平衡时O2的浓度:乙>甲
C. 平衡时SO2的转化率:乙>甲
D. 平衡时SO2的体积分数:乙>甲
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。
I、实验室采用气相还原法制备纳米级Fe,其流程如图所示:
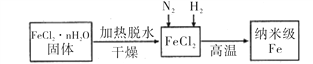
(1)纳米级Fe和稀盐酸反应的离子方程式为_______________________________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2 _____________________________________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为______________________________________。
II、查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。甲同学用如图甲装置所示进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是 ______________________。
(5)甲装置中仪器a的名称为_______________________。
(6)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
实验步骤 | 实验操作 | 实验现象 |
I | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
II | 向实验I得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。
丙同学认为乙同学的结论不正确,他的理由是______(用简要文字描述)。
(7)丁同学称取5.60gFe粉,用乙装反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为________(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M的合成路线如下图所示:
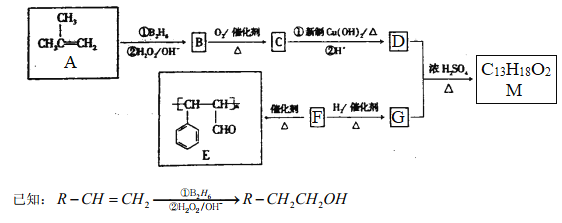
请回答下列问题:
(1)有机物A的系统命名为___________。
(2)F→E的反应类型为_________;B中所含官能团的名称为___________。
(3)M的结构简式为___________。
(4)C与新制Cu(OH)2悬浊液反应的化学方程式为___________。
(5)F有多种同分异构体,其中含苯环且与F所含官能团相同的同分异构体有_____种。
(6)参照M的合成路线,设计一条由丙烯和乙醇为起始原料制备丙酸乙酯的合成路线(无机试剂任选)___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不符合ⅦA族元素性质特征的是( )
A.从上到下原子半径逐渐减小
B.易形成﹣1价离子
C.最高价氧化物的水化物显酸性
D.从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要用 NaOH 固体配制 80mL 1.00mol·L-1 的 NaOH 溶液,试回答下列各题:
(1)人们常将配制过程简述为以下各步骤:
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移溶液 其正确的操作顺序应是_____________________(填各步骤序号)。
(2)在称量时,用托盘天平准确称量_____g 固体 NaOH;
(3)本实验必须用到的仪器有天平、药匙、烧杯、玻璃棒,还需要的仪器是_____。
(4)定容的操作要点是:__________。
(5) 配置过程中,以下操作会使 NaOH 溶液物质的量浓度偏高的是_____。
A.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
B.定容时俯视刻度线
C.往容量瓶转移时,有少量 NaOH 液体溅出
D.容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
F.向容量瓶中转移溶液时,未等溶液冷却就进行定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,下列操作或发生事故时的处理方法正确的是
A. 可用燃着的酒精灯引燃另一只酒精灯。
B. 给试管里的液体加热时,试管应与桌面垂直。
C. 配置一定浓度的NaCl溶液时,定容振荡摇匀后,发现液面低于刻度线,再加水到刻度线。
D. 浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,最后涂上3%-5%的小苏打溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定量的液态化合物XY2,在一定量的氧气中恰好完全燃烧,其化学方程式:XY2(l)+3O2(g)![]() XO2(g)+2YO2(g) (l代表液体,g代表气体)
XO2(g)+2YO2(g) (l代表液体,g代表气体)
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56 g·L-1。
(1)观察反应前后气体的化学计量数,可得反应前氧气的体积是__________。
(2)化合物XY2的摩尔质量是__________。
(3)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为__________和__________(填元素符号)。
II.常温下,将20.0 g质量分数为14.0 %的KNO3溶液跟30.0 g质量分数为24.0 %的KNO3溶液混合,得到密度为1.15 gcm﹣3的混合溶液。计算:
(1)混合后溶液的质量分数___________。
(2)混合后溶液的物质的量浓度____________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2=2Fe3++2H2O
C. 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D. 电解MgCl2水溶液的离子方程式:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com