
【题目】聚乙炔能够导电,下列关于聚乙炔![]() 和聚合物A
和聚合物A![]() 的说法中正确的是
的说法中正确的是
A. 聚合物A和聚乙炔均能使溴水褪色
B. 两种聚合物的单体互为同系物
C. 聚合物A的相对分子质量是聚乙炔的两倍
D. 1mol 两种聚合物的单体分别与Br2发生反应,最多消耗Br2的物质的量之比为2:1
科目:高中化学 来源: 题型:
【题目】以黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备二氧化氯气体,再用水吸收获得二氧化氯溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2气体的吸收率。具体情况如下图所示。
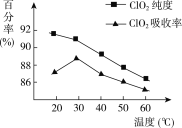
请回答下列问题:
(1)据图可知,反应时需要控制的适宜温度是________ ℃,达到此要求采取的适宜措施是________。
(2)已知:黄铁矿中的硫元素在酸性条件下被ClO3-氧化成SO42-,写出制备二氧化氯的离子方程式:____________________________________。
(3)某校化学学习小组拟以“m(ClO2)/m(NaClO3)”作为衡量ClO2产率的指标。若取NaClO3样品质量6.0 g,通过反应和吸收可得400 mL ClO2溶液,取出20 mL,加入37.00 mL 0.500 mol·L-1(NH4)2Fe(SO4)2溶液充分反应,过量Fe2+再用0.0500 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗20.00 mL。反应原理如下:
4H++ClO2+5Fe2+===Cl-+5Fe3++2H2O
14H++6Fe2++Cr2O72-===2Cr3++6Fe3++7H2O
试计算ClO2的“产率”为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,不正确的是( )
A.用托盘天平称取 4.5 g 固体氯化钠B.在烧杯中稀释浓硫酸
C.用温度计代替玻璃棒搅拌溶液D.在蒸发皿中蒸发浓缩食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X的化学式是________。
(2)固体甲与稀硫酸反应的离子方程式是___________。
(3)加热条件下氨气被固体X氧化成一种气体单质,写出该反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是Na202和C02定性、定量实验的装置示意图。
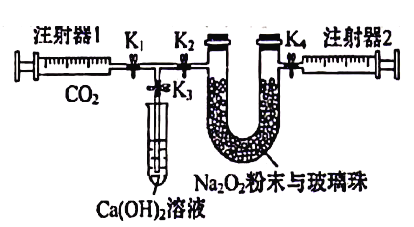
注射器1中抽取了100mL CO2,U型管中装有适量小玻璃珠和约1.5g Na2O2粉末。实验开始时,打开K1、K2、K4止水夹,关闭K3止水夹,推动注射器1活塞,缓缓将CO2压至U型管,注射器2活塞缓缓向外移动。下列叙述中不正确的是
A. U形管内的玻璃珠可防止过氧化钠粉末被吹和增大过氧化钠和二氧化碳的接触面积
B. U形管内淡黄色粉末渐渐变白
C. 注射器1活塞推到底后,注射器2中收集到的气体大于50mL,只是因为还含有CO2
D. 打开胶塞,立即将带火星的木条伸入U形管中,可验证反应产物之一为氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有1molHNO3和1molH2OS4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是()
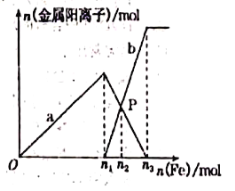
A. a表示n(Fe3+)的变化曲线
B. n1=0.75
C. P点时,n(Fe2+)=0.5625 mol
D. 向P点溶液中加入铜粉,最多可溶解14.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.
根据图示回答下列问题:

(1)写出A、B、C、D、E的结构简式:A_____,B_____,C_____,D_____,E_____;
(2)写出②、④两步反应的化学方程式:
②_________________________________;
④__________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com