
| A. | 丁烷 | B. | 1,3-丁二烯 | ||
| C. | 乙苯 | D. | 2-甲基-1,3-丁二烯 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A.丁烷中,2号碳原子连接的四个原子是四面体结构,其中3个碳原子形成一个平面,4号碳原子位于该平面的外部,所以共面的碳原子数有3个;
B.乙烯为平面结构,CH2=CH-CH=CH2中所有碳原子可能都处在同一平面上,所以共面的碳原子数最多有4个;
C.苯为平面结构,乙苯中所有碳原子可能都处在同一平面上,所以共面的碳原子数最多有8个;
D.乙烯为平面结构,CH2=C(CH3)-CH=CH2中所有碳原子可能都处在同一平面上,所以共面的碳原子数最多有5个;
故选C.
点评 本题主要考查有机化合物的结构特点,难度不大,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 达到化学反应限度时,生成2mol NH3 | |
| B. | 向容器中再加入N2,可以加快反应速率 | |
| C. | 降低温度可以加快反应速率 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的结构式:O=C=O | |
| B. | 硫酸的电离方程式:H2SO4=H++SO42- | |
| C. | Cl-的结构示意图: | |
| D. | HF的电子式:H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
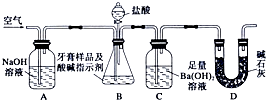 化学兴趣小组对某品牌牙膏中磨擦剂成分及其含量进行以下探究:
化学兴趣小组对某品牌牙膏中磨擦剂成分及其含量进行以下探究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
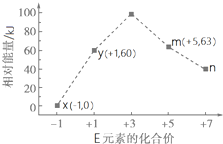 下表给出五种短周期元素的相关信息.
下表给出五种短周期元素的相关信息.| 元素 | 相关信息 |
| A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com