
【题目】下列3种有机化合物A: CH2=CH-CH3B:![]() C:CH3CH2OH
C:CH3CH2OH
(1)写出化合物A、C中的官能团的名称 、 。
(2)A在催化剂加热条件下生成聚合物的反应方程式为 。
(3) B可以被酸性高锰酸钾氧化成苯甲酸,写出苯甲酸与C物质在浓硫酸中共热发生酯化反应的化学方程式: 。
(4) 草酸(乙二酸)与乙二醇按1:1生成聚乙二酸乙二酯的反应方程式为__________。
(5) 苯酚钠中通入二氧化碳的反应方程式为__________________________________。
【答案】(1)碳碳双键,羟基;
(2) ;
;
(3)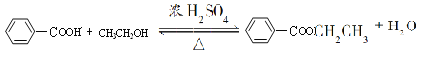 ;
;
(4)nHOOC-COOH+nHO-CH2CH2-OH![]() HO-[-OC-COO-CH2CH2-O-]n-H+(2n-1)H2O;
HO-[-OC-COO-CH2CH2-O-]n-H+(2n-1)H2O;
(5)CO2+H2O+C6H5ONa→C6H5OH + NaHCO3
【解析】试题分析:(1)化合物A、C中的官能团的名称分别为碳碳双键,羟基;
(2)A在催化剂加热条件下生成聚丙烯的反应方程式为 ;
;
(3)苯甲酸与C在浓硫酸中共热发生酯化反应的化学方程式为
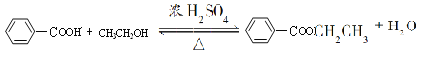 ;
;
(4)乙二酸与乙二醇按1:1生成聚乙二酸乙二酯的反应方程式为
nHOOC-COOH+nHO-CH2CH2-OH![]() HO-[-OC-COO-CH2CH2-O-]n-H+(2n-1)H2O;
HO-[-OC-COO-CH2CH2-O-]n-H+(2n-1)H2O;
(5)苯酚钠中通入二氧化碳的反应方程式为CO2+H2O+C6H5ONa→C6H5OH + NaHCO3 。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1)在298K,100kPa时.CH4的燃烧热是890.0kJ/mol,写出该反应的热化学方程式__________。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,共放出QkJ热量(假定热量未损失),则CH4和CO的物质的量的比为__________。
(2)利用甲烷的燃烧反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液.多孔石墨作电极,在电极上分别通入甲烷和氧气,通入甲烷气体的电极上发生的电极反应是___________,当电路中转移12mol电子时,实际提供的电能是890.0kJ,则该电池的能量转化效率是__________。
(3)将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:

①当开关K1闭合,则铁发生电化学腐蚀中的__________腐蚀。
②当开关K2闭合,则总反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。下列说法不正确的是
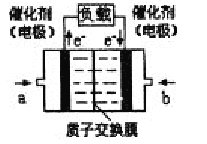
A.右电极为电池正极,b处通入的物质是空气
B.左电极为电池负极,a处通入的物质是空气
C.负极反应式为:CH3OH+H2O-6e—=CO2+6H+
D.正极反应式为:O2+4H++4e—=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在5 L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。起始反应时NO和CO各为3 mol,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
N2(g)+2CO2(g)。起始反应时NO和CO各为3 mol,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
A.达到平衡后,若将容器体积压缩为2 L,则正反应速率将增大,逆反应速率将减小
B.反应前5秒钟内,用CO表示的平均反应速率为0.04 mol·L-1·s-1
C.当v正(CO)=2v逆(N2)时,该反应中NO的物质的量不再改变
D.保持压强不变,往容器中充入1 mol He,正、逆反应速率都不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
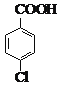
【题目】(14 分)对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应、装置图如下:
![]()
![]()
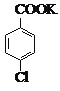 +MnO2
+MnO2 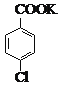
![]()
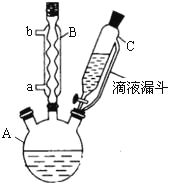
常温条件下的有关数据如下表所示:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 颜色 | 水溶性 | |
对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g。
请回答下列问题:
(1)装置B的名称是 。
(2)量取6.00mL对氯甲苯应选用的仪器是 。(填选仪器序号)
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是 。对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 。
(4)第一次过滤的目的是 ,滤液中加入稀硫酸酸化,可观察到的实验现象是 。
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是 。
(6)本实验的产率是 (填标号)。A.60% B.70% C.80% D.90%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、CO等大气污染气体的处理及利用的方法具有重要意义,可实现绿色环保、节能减排、废物利用等目的。
(1) 利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJmol﹣1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJmol﹣1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g),500℃时的平衡常数为9,若在该温度下进行,设起始时CO和H2O的起始浓度均为0.020 mol·L-1,则CO的平衡转化率为: 。
H2(g)+CO2(g),500℃时的平衡常数为9,若在该温度下进行,设起始时CO和H2O的起始浓度均为0.020 mol·L-1,则CO的平衡转化率为: 。
(3) 用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图1所示。
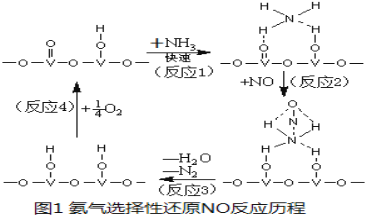
①写出总反应化学方程式 。
②测得该反应的平衡常数与温度的关系为:lgK=5.08+217.5/T,该反应是 反应(填“吸热”或“放热”)。
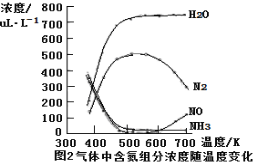
③该反应的含氮气体组分随温度变化如图2所示,当温度达到700K时,发生副反应的化学方程式 。
(4)下图是用食盐水做电解液电解烟气脱氮的一种原理图,NO被阳极产生的氧化性物质氧化为NO3—,尾气经氢氧化钠溶液吸收后排入空气。如下图,电流密度和溶液pH对烟气脱硝的影响。
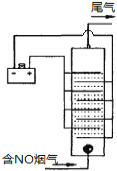
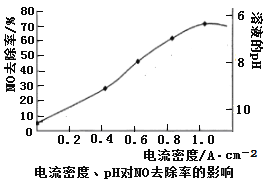
①NO被阳极产生的氧化性物质氧化为NO3-反应的离子方程式 。
②溶液的pH对NO去除率影响的原因是 。
③若极板面积10cm2,实验烟气含NO 1.5%,流速为0.070L·s-1(气体体积已折算成标准状态,且烟气中无其他气体被氧化),法拉第常数为96500 C·mol-1,测得电流密度为1.0 A·cm-2。列式计算实验中NO除去率 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为1/3Fe2O3(s)+CO(g) ![]() 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
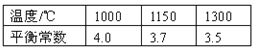
请回答下列问题:
(1)该反应的平衡常数表达式K= ,由于随着温度升高,平衡常数减小,所以正反应是 热反应(填“吸”或“放”);
(2)欲提高反应中CO的平衡转化率,可采取的措施是 ;
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.加入合适的催化剂
E.增大容器的容积
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,反应经过5min后达到平衡。求该时间范围内反应的平均反应速率:v (CO2)= 、CO的平衡转化率= 。(要书写解题过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
(1)x= 。
(2)平衡时C的浓度为多少?(要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下:
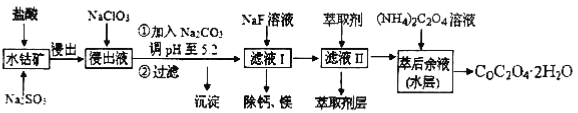
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

(1)浸出过程中加入Na2SO3的目的是_______________。
(2)NaClO3在反应中氯元素被还原为最低价,该反应的离子方程式为
____________________________________________________________________________
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀。试用离子方程式和必要的文字简述其原理:_______________________________________________________
(4)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液=______。
(5)萃取剂对金属离子的萃取率与pH的关系如右图所示,在滤液II中适宜萃取的pH为___左右。
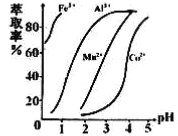
a.1 b.2 c.3 d.4
(6)已知:NH3·H2O![]() NH4++OH- Kb=1.8×10-5;
NH4++OH- Kb=1.8×10-5;
H2C2O4![]() H++HC2O4- Ka1=5.4×10-2;HC2O4-
H++HC2O4- Ka1=5.4×10-2;HC2O4-![]() H++C2O42- Ka2=5.4×10-5;
H++C2O42- Ka2=5.4×10-5;
则该流程中所用(NH4)2C2O4溶液的pH_____7(填“>”或“<”或“=”)
(7)CoC2O4·2H2O热分解质量变化过程如右图所示(其中600℃以前是隔绝空气加热,,600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是__________
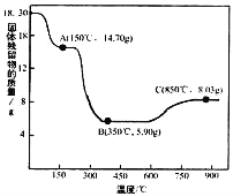
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com