
| A、NaAlO2溶液中滴加过量盐酸:AlO2-+H2O+H+=Al(OH)3 | ||||
B、NH4HSO3溶液与足量浓NaOH溶液共热:NH4++HSO3-+2OH-
| ||||
| C、明矾溶于水产生Al(OH)3 胶体:Al3++3H2O=Al(OH)3↓+3H+ | ||||
| D、FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ |
| ||


科目:高中化学 来源: 题型:

| A、图1所示的总反应为吸热反应 |
| B、图2表示常温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
| C、图3表示反应CO(g)+2H2(g)?CH3OH(g)平衡常数K随CO浓度变化的关系 |
| D、图4可以说明在恒容密闭容器中充入SO2、O2,反应2SO2(g)+O2(g)═2SO3(g) 从t1时刻起达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 锰及其化合物在现代工业及国防建设中具有十分重要的地位.
锰及其化合物在现代工业及国防建设中具有十分重要的地位.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液:Ca2+、H+、Cl-、HSO3- | ||
B、
| ||
| C、Na2CO3溶液:K+、Na+、SO42--、AlO2- | ||
| D、能使PH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
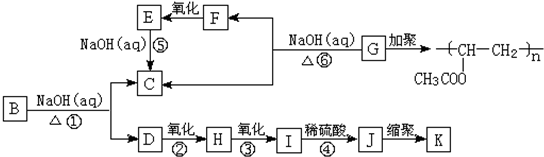
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com