
| A. | 石油经分馏得到的各馏分仍然是多种烃的混合物 | |
| B. | 石油分馏的目的是将含碳原子数较多的烃先气化,经冷凝而分离出来 | |
| C. | 石油经过分馏、裂化等工序后得到大量乙烯、苯等不饱和烃 | |
| D. | 石油的炼制过程是将相对分子质量较大分子变成相对分子质量较小分子的过程 |
分析 A.分馏石油得到的各个馏分中含有多种烃类物质;
B.根据石油分馏原理以及碳原子数少的烃沸点低;
C.依据石油裂解产品解答;
D.石油炼制包括:石油的分馏、石油裂化和石油裂化等.
解答 解:A.分馏石油得到的各个馏分中含有多种烃类物质,属于混合物,故A正确;
B.石油分馏的目的是将含碳原子数较小的烃先气化,经冷凝而分离出来,故B错误;
C.石油裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯、乙炔等,裂化不能得到大量乙烯、苯等不饱和烃,故C错误;
D.石油炼制过程中,利用石油中各成分的沸点不同,将它们分馏可得到汽油、煤油、柴油、润滑油、沥青等等不同产品;石油的裂化是在一定条件下,将相对分子质量较大,沸点较高的烃分解为相对分子质量较小、沸点较低的烃;石油裂解为高于裂化温度下深度裂化,以石油分馏产品为原料,裂解所得产物主要是乙烯、丙烯等小分子化合物,故D错误;
故选:A.
点评 本题考查了石油的炼制,明确石油的成分及石油的分馏、裂解、裂化原理及产品是解题关键,题目难度不大,注意对基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 37% | ||
| C. | 50% | D. | 数据不全无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸检测,氨水溶液呈碱性:NH3•H2O=NH4++OH- | |
| B. | 100℃时,测得纯水中c(H+)•c(OH-)=3.8×10-13 H2O(l)?H+(aq)+OH-(aq)△H<0 | |
| C. | FeCl3溶液中通入适量SO2,溶液黄色褪去:Fe3++SO2+2H2O=Fe2++SO42-+4H+ | |
| D. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表第5列是第Ⅴ副族 | |
| B. | 元素周期表中所含元素种类最多的族是第Ⅷ族 | |
| C. | 第ⅠA族的元素就是碱金属元素 | |
| D. | 元素周期表中第4、5、6、7周期为长周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打雷闪电时,大气中产生了NO | |
| B. | 豆科植物的根瘤菌把空气中的氮气转化为硝酸盐等含氮化合物 | |
| C. | N2和H2在一定条件下反应生成NH3 | |
| D. | NH3经催化氧化生成NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通入足量氢氧化钠溶液中:CO2+2OH-=CO32-+H2O | |
| B. | 用小苏打治疗胃酸过多:HCO${\;}_{3}^{-}$+OH-=CO2↑+H2O | |
| C. | 将Cl2通入水中:Cl2+H2O=Cl-+2H++ClO- | |
| D. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
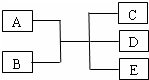 己知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,
己知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
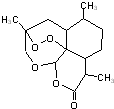 2015年10月,我国85岁高龄的女科学家屠呦呦因发现青蒿素为治疗疟疾做出了突出贡献,被授予诺贝尔医学奖.青蒿素结构如图所示,下列关于青蒿素的说法错误的是
2015年10月,我国85岁高龄的女科学家屠呦呦因发现青蒿素为治疗疟疾做出了突出贡献,被授予诺贝尔医学奖.青蒿素结构如图所示,下列关于青蒿素的说法错误的是| A. | 不易溶于水 | |
| B. | 分子式是C15H22O5 | |
| C. | 1mol青蒿素能与1mol NaOH发生反应 | |
| D. | 能发生加成反应,不能发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com