
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
分析 ①碳酸根离子水解生成碳酸氢根离子和氢氧根离子;
②铵根离子水解生成一水合氨和氢离子;
③铜离子水解生成氢氧化铜和氢离子;
④氟离子水解生成氟化氢和氢氧根离子,水解反应为可逆反应.
解答 解:①碳酸钠溶液中,碳酸根离子水解分步进行,主要以第一步为主,碳酸根离子水解的方程式为:CO32-+H2O?HCO3-+OH-,故错误;
②铵根离子水解的离子方程式为:NH4++H2O?NH3•H2O+H+,故正确;
③铜离子水解生成氢氧化铜,铜离子水解方程式为:Cu2++2H2O?Cu(OH)2+2H+,故正确;
④水解反应为可逆反应,应该用可逆号,氟离子水解的方程式为:F-+H2O?HF+OH-,故错误.
故选B.
点评 本题考查了水解的离子方程式的正误判断,为高频考点,侧重考查学生的分析能力,题目难度中等,注意明确盐的水解原理,明确水解反应为可逆反应,多元弱酸根离子的水解分步进行,主要以第一步为主.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 锌片插入硝酸银溶液中:Zn+Ag+═Zn2++Ag | |
| B. | 硫化钠溶液中通入足量二氧化硫:2S2-+5SO2+2H2O═3S↓+4HSO3- | |
| C. | 碳酸氢镁溶液中滴入足量氢氧化钠溶液:Mg2++HCO3-+OH-═Mg CO3↓+H2O | |
| D. | 碳酸氢钙溶液加到醋酸中:HCO3-+H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
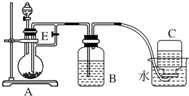 如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑、4mol•L-1的硫酸溶液,其他试剂任选.填写下列空白.
如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑、4mol•L-1的硫酸溶液,其他试剂任选.填写下列空白.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④⑤⑦ | C. | ③④⑥ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA | |
| B. | 2.24 L二氧化碳中含有共价键数目为4NA | |
| C. | 7.1g Cl2与足量NaOH 溶液反应转移的电子数为0.2NA | |
| D. | 1 mol NH4+中含有电子数为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 起始浓度/mol•L-1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | X | 0.2 | 7 |
| A. | 实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) | |
| B. | 实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=$\frac{{K}_{W}}{1×1{0}^{-5}}$mol•L-1 | |
| C. | 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol•L-1 | |
| D. | 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com