
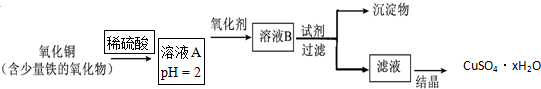
分析 用含少量铁的氧化物的氧化铜加入稀硫酸可得到溶液A含有Fe3+、Fe2+、Cu2+,调节溶液pH=2并加入氧化剂可将Fe2+氧化生成Fe3+,加入试剂CuO、Cu(OH)2 或Cu2(OH)2CO3,调节溶液pH使Fe3+生成氢氧化铁沉淀而除去,过滤后滤液为硫酸铜溶液,经蒸发结晶可得到硫酸铜晶体,以此解答该题.
解答 解:用含少量铁的氧化物的氧化铜加入稀硫酸可得到溶液A含有Fe3+、Fe2+、Cu2+,调节溶液pH=2并加入氧化剂可将Fe2+氧化生成Fe3+,加入试剂CuO、Cu(OH)2 或Cu2(OH)2CO3,调节溶液pH使Fe3+生成氢氧化铁沉淀而除去,过滤后滤液为硫酸铜溶液,经蒸发结晶可得到硫酸铜晶体,
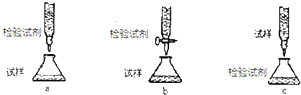
(1)Fe2+具有还原性,可被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,与KSCN不反应,加入硫化铵、氢氧化钠溶液可生成CuS、氢氧化铁、氢氧化铜沉淀而不能检验Fe2+,只有a正确,
故答案为:a;
(2)用高锰酸钾测定溶液A中Fe2-的浓度,因高锰酸钾具有强氧化性,应放在酸式滴定管中,发生反应的离子式为5Fe2++MnO4-+8H+=5Fe3++Mn2++2H2O,
故答案为:b;5Fe2++MnO4-+8H+=5Fe3++Mn2++2H2O;
(3)溶液B中含有Fe3+、Cu2+,为除去Fe3+,可加入试剂CuO、Cu(OH)2 或Cu2(OH)2CO3,调节溶液pH使Fe3+生成氢氧化铁沉淀而除去,避免引入新杂质,
故答案为:cde;
(4)称取mg硫酸铜晶体,加入足量氢氧化钠溶液生成氢氧化铜、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,最后得到沉淀为CuO,质量为ng,则n(CuO)=$\frac{n}{80}$mol,
则n(CuSO4)=n(CuO)=$\frac{n}{80}$mol,
m(CuSO4)=$\frac{n}{80}$mol×160g/mol=2ng,
m(H2O)=(m-2n)g,
n(H2O)=$\frac{m-2n}{18}$mol,
x=$\frac{n({H}_{2}O)}{n(CuS{O}_{4})}$=$\frac{\frac{m-2n}{18}}{\frac{n}{80}}$=$\frac{40(m-2n)}{9n}$,
故答案为:$\frac{40(m-2n)}{9n}$.
点评 本题考查物质的制备,为高频考点和常见题型,侧重于学生的分析、实验和计算能力得到考查,注意把握实验的原理以及物质的性质,为解答该类题目的关键,注意掌握实验基本操作和流程分析,题目难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | △H=-600.4kJ/mol | B. | △H=-1081.6kJ/mol | ||
| C. | △H=+90.8kJ/mol | D. | △H=-90.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2mL,NO | B. | 2.4mL,O2 | C. | 3.5mL O2 | D. | 4mL,NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
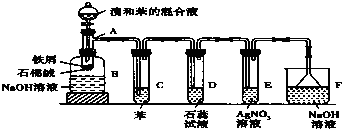
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
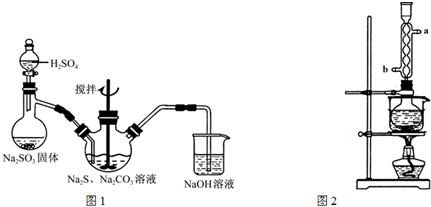
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
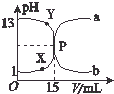 如图曲线a和b是盐酸与氧氧化钠溶液在常温下的相互滴定的滴定曲线,下列叙述中正确的是( )
如图曲线a和b是盐酸与氧氧化钠溶液在常温下的相互滴定的滴定曲线,下列叙述中正确的是( )| A. | 盐酸的物质的量浓度为1 mol•L-1 | |
| B. | P点时反应恰好完成,溶液呈中性,但它不是滴定终点 | |
| C. | X点时c(Cl-)>c(H+)>c(Na+)>c(OH-) | |
| D. | Y点时溶液呈碱性,溶液中c(H+)•c(OH-)>1×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com