
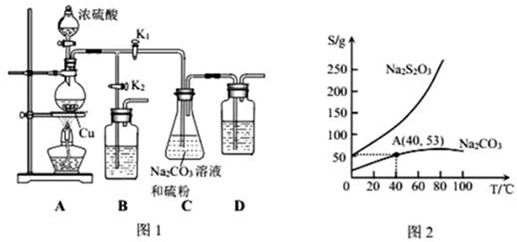
分析 (1)由于浓硫酸和Cu片反应产生的SO2与C中的物质反应会有过量,B和D是为了吸收多余的二氧化硫;C中二氧化硫与碳酸钠以及硫混合反应生成Na2S2O3和二氧化碳,据此书写方程式;
(4)由图象2可知,40℃Na2CO3的溶解度为53g,所以50g水中有Na2CO3的物质的量为$\frac{\frac{53}{2}}{106}$=0.25mol,结合C中的反应:SO2+Na2CO3+S=Na2S2O3+CO2进行计算.
解答 解:(1)由于浓硫酸和Cu片反应产生的SO2与C中的物质反应会有过量,所以B和D可以用来吸收过量的SO2尾气,防止污染环境;C中通入的二氧化硫与碳酸钠以及硫混合反应生成Na2S2O3和二氧化碳,方程式为:SO2+Na2CO3+S=Na2S2O3+CO2;故答案为:吸收过量的SO2尾气,防止污染环境;SO2+Na2CO3+S=Na2S2O3+CO2;
(4)由图象2可知,40℃Na2CO3的溶解度为53g,所以50g水中有Na2CO3的物质的量为$\frac{\frac{53}{2}}{106}$=0.25mol,又根据C中的反应:SO2+Na2CO3+S=Na2S2O3+CO2可知,Na2CO3完全反应,所以Na2S2O3生成0.25mol,故可得Na2S2O3•5H2O质量为0.25mol×208g/mol=62g,故答案为:62.
点评 本题考查化学实验的制备、含量测定,涉及对尾气吸收、方程式的书写化学计算等知识,是对学生综合能力的考查,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 被测样品中含有加热不挥发的杂质 | B. | 被测样品中含有加热易挥发的杂质 | ||
| C. | 实验前被测样品已有部分失水 | D. | 加热前所用的坩埚未完全干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
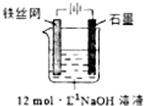 高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.
高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
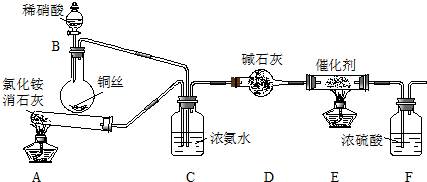
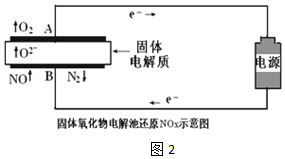
| 实验序号 | B极气体 | 电路中通过电子 | 消耗总电能 | 生成N2 |
| 实验1 | NO | 1mol | a KJ | 0.25mol |
| 实验2 | NO和空气 (不考虑NO2) | 1mol | a KJ | 0.09mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 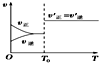 反应H2(g)+I2(g)?2HI(g)达到平衡后,升高温度时反应速率随时间的变化 | |
| B. | 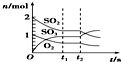 反应2SO2(g)+O2(g)?2SO3(g)达到平衡后,缩小容器容积时各成分的物质的量随时间的变化 | |
| C. |  反应N2(g)+3H2(g)?2NH3(g)在恒温条件下,反应速率与压强的关系 | |
| D. |  反应CO2(g)+H2(g)?CO(g)+H2O(g)△H>0水蒸气含量随时间的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
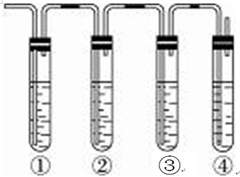 实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫.A.品红溶液 B.NaOH溶液 C.浓硫酸 D.高锰酸钾酸性溶液.试完成下列问题:
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫.A.品红溶液 B.NaOH溶液 C.浓硫酸 D.高锰酸钾酸性溶液.试完成下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com