
| A、硫酸 | B、氨水 |
| C、盐酸 | D、氢氧化钠 |


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中一定有CO32- |
| B、用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是排除SO42-以外的其它阴离子及Ag+的干扰 |
| C、做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待测溶液进行实验 |
| D、验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 钢 | |||
| 碳素钢(Fe、C、Mn、Si) | 合金钢 | ||
| 低碳钢 | 中碳钢 | 高碳钢 | 碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% | 含碳量0.3%~0.6% | 含碳量>0.6% | |
| 韧性好,强度低 | 韧性好、强度好 | 硬而脆 | 具有特殊性能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
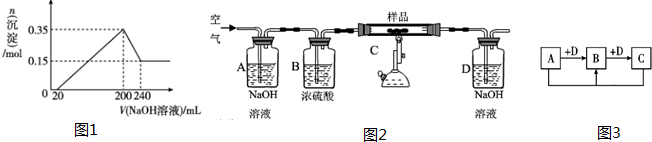
| A、现象相同,最终沉淀量相等 |
| B、现象不同,最终沉淀量不相等 |
| C、现象相同,最终沉淀量不相等 |
| D、现象不同,最终沉淀量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热的纯碱溶液可以去除油污 |
| B、金属钠可以从硫酸铜溶液中置换出铜 |
| C、碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一 |
| D、镁燃烧发出耀眼的白光,常用来制造信号弹和焰火 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶、烧杯、量筒使用前均需要验漏、洗净并烘干 |
| B、分液时,需先打开分液漏斗上端的玻璃塞,再将下层液体从下口放出 |
| C、将硫酸铜溶液蒸发至有大量固体析出时,停止加热,便可得到胆矾晶体 |
| D、配制一定物质的量浓度溶液时,当容量瓶中液面高于刻度线时,用胶头滴管吸出少量液体即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、给与水的反应:Na+H2O=Na++OH-+H2↑ |
| B、氯化铝溶液中满加过量氯水:Al3++4NH3?H2O=[Al(OH)4]++4NH4+ |
| C、硅酸钠溶液中通入过量二氧化碳:SiO32-+CO2+H2O=H2SiO3↓+CO32- |
| D、AgCl悬浊液中滴加KI,现现黄色沉淀:AgCl(s)+I-(aq)=AgI(s)+Cl-(aq) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com