
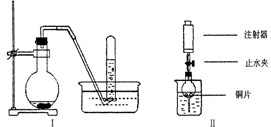
 某同学甲采用如下图I所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体.
某同学甲采用如下图I所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体.

 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 每100g含有 营养成分 |
糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
| 纤维编号 | ① | ② | ③ |
| 灼烧时的气味 | 特殊气味 | 烧纸气味 | 烧焦羽毛气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能(kJ?mol-1) | 348 | 413 | 436 | 358 | 750 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molH2O所含有的原子数为NA |
| B、常温常压下,32gO2含有的氧原子数为2NA |
| C、常温常压下,11.2 L氯气所含的分子数为NA |
| D、1L0.1mol/L NaCl 溶液中所含的Na+为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com