
| A、7 g CnH2n中含氢原子数为NA | ||||
| B、4.6 g SO2、CO2混合气体中含有中子数为2.3NA | ||||
C、在反应2Na2O2+2 CO2
| ||||
| D、电解精炼铜时每转移NA个电子,阳极溶解32 g铜 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、己烯、甲苯、苯酚溶液 |
| B、己烷、苯、四氯化碳 |
| C、庚烷、1-庚烯、1,2-二溴乙烷 |
| D、苯、酒精、硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和NH4+是等电子体,化学键类型完全相同 |
| B、NO3-和CO32-是等电子体,均为平面正三角形结构 |
| C、H3O+和PCl3是等电子体,均为三角锥形结构 |
| D、SO2和O3是等电子体,SO2和O3具有相同的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,28g氮气所含有的原子数目为NA |
| B、1molNa被完全氧化生成Na2O2,失去电子数目为NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、56 g Fe与任何物质完全反应时转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、X、Y、Z离子半径依次增大 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、W、X、Z对应气态氢化物稳定性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
| B、用100 mL量筒测得排水法收集制得的氢气体积为50.28 mL |
| C、用广泛PH试纸测得某雨水的PH为5.6 |
| D、做过焰色反应的金属丝应用稀盐酸洗,再灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
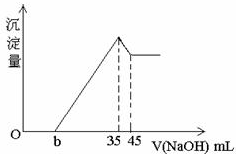 取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )| A、A、1mol/L |
| B、B、1.75mol/L |
| C、C、3.5mol/L |
| D、D、2mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com