

| A. | 1mol该物质最多可与2molH2发生加成反应 | |
| B. | 该物质的分子式为C9H8O | |
| C. | 加热时,该物质能与新制Cu(OH)2悬浊液反应 | |
| D. | 该物质既能发生加成反应,也能发生取代反应 |
分析 根据有机物的结构简式判断有机物含有的原子个数,可确定有机物的分子式,含有C=C,可发生加成、加聚、氧化反应,含有醛基,可发生加成、氧化反应,以此解答该题.
解答 解:A.能与氢气发生加成反应的为醛基、碳碳双键和苯环,则1mol该物质最多可与5molH2发生加成反应,故A错误;
B.由结构简式可知有机物分子式为C9H8O,故B正确;
C.含有醛基,可与氢氧化铜浊液在加热条件下发生氧化还原反应,故C正确;
D.含有醛基、碳碳双键,可发生加成反应,苯环可发生取代反应,故D正确.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重醛、烯烃性质的考查,题目难度不大.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,同一时间内阳极溶解铜的质量比比阴极析出铜的质量小 | |
| B. | 高炉炼铁时,增加高炉高度,延长CO和铁矿石的接触时间,可以提高CO利用率 | |
| C. | 硫酸工业中,接触室内安装热交换器,是为了将SO2完全转化为SO3 | |
| D. | 侯氏制碱是将CO2和NH3先后通入饱和氯化钠溶液中得碳酸氢钠固体,再灼烧制碳酸钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
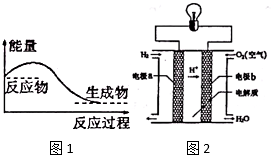 能盘是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.
能盘是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜片表面有气泡生成 | |
| B. | 该装置能使化学能直接转变为光能 | |
| C. | 如果将硫酸换成CuSO4溶液,导线中不会有电子流动 | |
| D. | 电路中电子的流动方向是Cu→Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na[Au(CN)2]可溶于水 | |
| B. | 化合物Na[Au(CN)2]中金元素的化合价为+2 | |
| C. | 金化学性质稳定,不与任何物质反应 | |
| D. | 在提炼过程中含金元素的物质始终作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
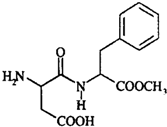 阿斯巴甜具有清爽的甜味,甜度约为蔗糖的200倍,其结构简式如图所示.下列关于阿斯巴甜的说法错误的是( )
阿斯巴甜具有清爽的甜味,甜度约为蔗糖的200倍,其结构简式如图所示.下列关于阿斯巴甜的说法错误的是( )| A. | 阿斯巴甜属于糖类 | |
| B. | 在一定条件下完全水解,产物中有两种氨基酸 | |
| C. | 既能与酸反应又能与碱反应 | |
| D. | 可发生取代反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
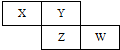 X、Y、Z、W四种短周期元素在周期表中的位置关系如图
X、Y、Z、W四种短周期元素在周期表中的位置关系如图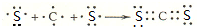 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置a烧瓶内加入的固体可以是MnO2 | |
| B. | 若按a、e、d、b、c顺序连接装置,则e中盛装的是浓硫酸 | |
| C. | 制备过程中装置b硬质玻璃管内有红棕色的烟产生 | |
| D. | 验证产物中的Fe3+存在可使用KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com