
| A. | 8.2L | B. | 11.5L | C. | 15.7L | D. | 16.8L |
分析 利用极限法解答:假设混合物全为CuS,或混合物全为Cu2S,根据n=$\frac{m}{M}$计算出n(CuO),利用原子守恒计算出n(CuS)、n(Cu2S),再根据电子守恒计算出n(NO)、n(NO2),然后根据V=nVm计算出混合气体体积,实际的气体体积介于二者之间.
解答 解:①若混合物全是CuS,其物质的量n(CuS)=n(CuO)=$\frac{12g}{80g/mol}$=0.15mol,转移电子物质的量=0.15×(6+2)=1.2mol,NO和NO2的体积相等,
设NO的物质的量为x、NO2的物质的量为x,
则:3x+x=1.2,
解得:x=0.3,
则生成混合气体的体积为:0.6mol×22.4L/mol=13.44L;
②若混合物全是Cu2S,其物质的量n(Cu2S)=$\frac{1}{2}$n(CuO)=$\frac{1}{2}$×0.15mol=0.075mol,转移电子物质的量为:0.075×10=0.75mol,
设NO为xmol、NO2为xmol,3x+x=0.75,
解得:x=0.1875,
生成气体体积为:0.1875mol×2×22.4L/mol=8.4L,
由于是CuS和Cu2S的混合,则生成的气体体积介于8.4L~13.44L之间,满足条件的为B,
故选B.
点评 本题考查化合物反应的计算、氧化还原反应的计算,题目难度中等,注意掌握守恒思想与极限法的利用,试题侧重对学生综合能力的考查,有利于提高学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 溶液的导电性与溶液中离子的浓度有关 | |
| B. | 溶液的导电性与溶液中离子数目的多少有关 | |
| C. | 灯泡最暗时溶液中无自由移动的离子 | |
| D. | 往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 生成物是HI和HClO | B. | 生成物是HCl和HIO | ||
| C. | 属于置换反应 | D. | 属于复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
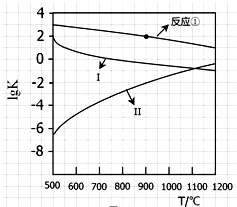 用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应.
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质生成的分解反应一定是氧化还原反应 | |
| B. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| C. | 氧化剂被氧化,还原剂被还原 | |
| D. | 没有氧元素参加的反应一定不是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com