
分析 处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、泡利不相容原理和洪特规则,根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写.
(1)Li元素为3号元素,原子核外有3个电子,分两层排布;
(2)Na元素为11号元素,原子核外有11个电子,分三层排布;
(3)Fe元素为26号元素,原子核外有26个电子,分四层排布;
(4)Ar元素为18号元素,原子核外有18个电子,分三层排布;
(5)铁原子失去最外层4s能级2个电子,形成Fe2+;核外电子排布式为:1s22s22p63s23p63d5;
(6)Cr元素为24号元素,原子核外有24个电子,分四层排布.
解答 解:(1)Li元素为3号元素,原子核外有3个电子,分两层排布,所以核外电子排布式为:1s22s1,
故答案为:1s22s1;
(2)Na元素为11号元素,原子核外有11个电子,分三层排布,所以核外电子排布式为:1s22s22p63s1,
故答案为:1s22s22p63s1;
(3)Fe元素为26号元素,原子核外有26个电子,分四层排布,所以核外电子排布式为:1s22s22p63s23p63d64s2,
故答案为:1s22s22p63s23p63d64s2;
(4)Ar元素为18号元素,原子核外有18个电子,分三层排布,所以核外电子排布式为:1s22s22p63s23p6,
故答案为:1s22s22p63s23p6;
(5)铁原子失去最外层4s能级2个电子,形成Fe2+,核外电子排布式为:1s22s22p63s23p63d6;
故答案为:1s22s22p63s23p63d6;
(6)Cr元素为24号元素,原子核外有24个电子,其电子排布式为1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1.
点评 本题考查了基态原子的核外电子排布式,根据核外电子排布规律来写,注意电子处于全满、半满、全空时最稳定,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | n1=n2 | B. | n1>n2 | C. | n1<n2 | D. | c(A-)<c(B-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的CH3COONa固体 | ||
| C. | 加入等体积0.2 mol•L-1盐酸 | D. | 提高溶液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式是 | |
| B. | 硝基苯的结构简式  | |
| C. | CH3CH(CH3)CH=CH2的名称 3-甲基-1-丁烯 | |
| D. | 甲烷分子的比例模型  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中NaOH的物质的量 | B. | 溶液中Na+的物质的量浓度 | ||
| C. | 溶液中Na+的数目 | D. | 溶液的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
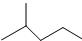 表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.
表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.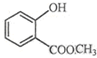 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com