
【题目】10g碳酸钙与足量盐酸反应,消耗盐酸的物质的量为多少?生成二氧化碳气体的体积(标准状况)为多少?(要求:写出化学反应方程式进行列式计算)
【答案】解:10g碳酸钙物质的量为:n( CaCO3)= ![]() =0.1mol,设消耗HCl物质的量为x,生成二氧化碳物质的量为y,
=0.1mol,设消耗HCl物质的量为x,生成二氧化碳物质的量为y,
CaCO3+ | 2HCl | ═ | CaCl2+ | H2O+ | CO2↑ |
1 | 2 | 1 | |||
0.1mol | x | y |
则:x= ![]() =0.2mol,y=
=0.2mol,y= ![]() =0.1mol
=0.1mol
所以消耗HCl的物质的量为0.2mol,标况下生成二氧化碳的体积为:0.1mol×22.4L/mol=2.24L,
答:消耗HCl的物质的量为0.2mol,标况下生成二氧化碳气体的体积为2.24L
【解析】发生反应为:CaCO3+2HCl═CaCl2+H2O+CO2↑,根据n= ![]() 计算碳酸钙物质的量,根据方程式计算消耗HCl物质的量、生成二氧化碳物质的量,再根据V=nVm计算二氧化碳的体积.
计算碳酸钙物质的量,根据方程式计算消耗HCl物质的量、生成二氧化碳物质的量,再根据V=nVm计算二氧化碳的体积.


科目:高中化学 来源: 题型:
【题目】葡萄酒中常加入亚疏酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通常以酒样中SO2的量计),某研究小组设计了如下实验(已知还原性:SO32->I->Cl-)。
![]()
下列说法不正确的是
A. 若试剂A选择氯水,则试剂B可选择NaOH标准液
B. 通入N2和煮沸的目的是为了将产生的气体从溶液中全部赶出
C. 葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
D. 若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I2标准液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列事实,能确定某晶体一定是离子晶体的是( )
A.晶体熔点达2500℃B.固态时不导电,溶于水能导电
C.固态时不导电,熔融状态下能导电D.温度越高,溶解度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产和生活中使用非常广泛.
I、NaNO2外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.
(1)上述反应中用单线桥标出电子转移的方向和数目.
(2)某厂废液中,含有2%~5%的NaNO2 , 直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是 .
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(3)II.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.根据下列反应回答问题:
A.Na2O2+2HCl═2NaCl+H2O2
B.Ag2O+H2O2═2Ag+O2↑+H2O
C.2H2O2═2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
上述反应中,H2O2仅体现氧化性的反应是(填序号)
(4)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是
(5)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4﹣、H2O、Mn2+、H2O2、H+ . 已知该反应中H2O2只发生了如下过程:H2O2→O2 .
①将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中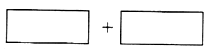
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,错误的是 ( )
A. 天然气的主要成分是CH4
B. 煤是由有机物和无机物组成的复杂的混合物
C. 淀粉、纤维素、蚕丝、油脂都是高分子化合物
D. 石油的分馏产品如汽油、煤油、柴油等都是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下对组成细胞和生物体的有机物的描述中,正确的是
A. 多肽链在核糖体上一旦合成便具有生物活性
B. 质量相同的糖、脂肪、蛋白质氧化分解所释放的能量是相同的
C. 细胞核内的核酸只含脱氧核糖,细胞质中的核酸只含核糖
D. 全部的抗体、绝大多数的酶、部分激素的化学本质是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠在供氧、防腐、除臭、微量分析等多方面有着重要用途,工业生产过氧化钠的方法是先将除去二氧化碳的干燥空气通入熔融的钠(温度453~473K) 中得到氧化钠,然后增加空气流量并迅速升高温度至573~673K 即可得到过氧化钠。某化学兴趣小组在实验室模拟工业流程制备过氧化钠,请回答下列相关问题。
(1)结合下图所示装置写出仪器连接顺序。

空气→______→______→______→______→______。(填导管口序号)_____________
(2)升温后发生的主要反应的化学方程式是_____________。
(3)下列选项中的加热方式适合该实验的是_____________(填选项序号)。
A.电炉 B.水浴 C.酒精喷灯 D.油浴(100-260℃ )
(4)若要提高产品纯度,需在具支试管后添加一个装置,该装置应该是_____________,其作用是_____________。
(5)实验中使用的钠的质量为4.600g,最终所得产品的质量为8.320g,通过仪器检测发现产品中含有少量NaN3,则该实验所得产品的产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉中加入少量稀硫酸,并加热。为了确定淀粉是否已水解或完全水解,需要①NaOH溶液;②银氨溶液;③新制Cu(OH)2碱性悬浊液;④碘水;⑤BaCl2中的
A.①⑤B.②④C.②③④D.①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com