
下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题。
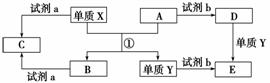
(1)请写出反应①的化学方程式:_________________________________________________。
(2)检验D溶液中Y离子的方法是______________________________________________。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式__________________。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是____________________________________。
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 L,则阴极产物的质量为__________________。
答案 (1)Fe2O3+2Al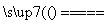 2Fe+Al2O3
2Fe+Al2O3
(2)取少量D溶液于试管中,滴加几滴KSCN溶液,若溶液变血红色,则证明有Fe3+
(3)2Al+2OH-+2H2O===2AlO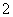 +3H2↑
+3H2↑
(4)2FeSO4+H2SO4+2NaNO2===2Fe(OH)SO4+Na2SO4+2NO↑
(5)54 g
解析 根据题意A为Fe2O3,X为Al,通过铝热反应生成氧化铝(B)和铁(单质Y);D与Fe反应生成E,则试剂b为非氧化性酸,D、E是Fe3+和Fe2+盐。
(4)E为FeSO4(铁的化合价为+2价)→Fe(OH)SO4(铁的化合价为+3价),而NaNO2(氮的化合价为+3价)→NO(氮的化合价为+2价)。根据电子得失守恒、质量守恒定律即可配平化学方程式。
(5)阳极反应:2O2--4e-===O2↑,标准状况下33.6 L的氧气物质的量为1.5 mol,转移电子数为6 mol,阴极反应:Al3++3e-===Al,故可以得到2 mol的Al,质量为2 mol×27 g·mol-1=54 g。


科目:高中化学 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH(固体) ②H2O ③HCl ④CH3COONa(固体)
A.②④ B.①④ C.②③ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下等物质的量浓度的下列溶液中,c(NH4+)最大的是( )
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D. (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是( )
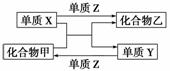
| 选项 | X | Y | Z | 甲 | 乙 |
| A | H2 | Si | Cl2 | SiCl4 | HCl |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上以金红石(主要成分是TiO2,主要杂质是SiO2)制取纳米级二氧化钛的流程如下:
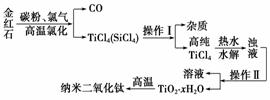
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70 ℃ | 57.6 ℃ |
| TiCl4 | -25 ℃ | 136.5 ℃ |
(1)写出氯化时生成TiCl4的化学方程式________________________。
(2)操作Ⅰ、操作Ⅱ名称分别是____________________、____________。
(3)写出TiCl4水解的化学方程式________________。
(4)如在实验室中完成灼烧TiO2·xH2O放在________(填字母序号)中加热。
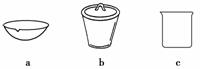
(5)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2。H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的________(填“氧化性”或“还原性”)。
(6)某研究小组用下列装置模拟“生态马路”的部分原理并测定CO的转化效率(夹持装置已略去)。
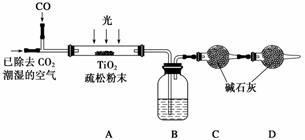
①B装置中的药品名称为________,若通入2.24 L(已折算成标准状况)CO气体和足量空气,最终测得装置A增重1.1 g,则CO的转化率为________。
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置能达到相关实验目的的是
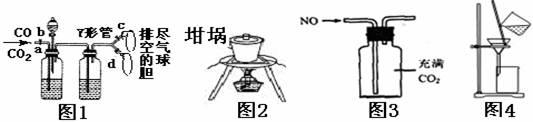
A.图1可用于分离收集CO和CO2 B.图2用于从食盐水中提取NaCl晶体
C.图3用于收集NO D.图4用于氢氧化铁胶体和硫酸钠溶液的分离
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、L四种元素分别位于周期表中三个紧相邻的周期且原子序数依次增大,它们相关信息如下:
X元素原子的价电子构型为nsnnp2n
Y和Z位于同一周期,最外层都有两个未成对电子
L元素原子的基态未成对电子数是同周期最多的元素。
请回答如下问题:
(1)L元素在周期表中的位置是 。
该原子核外电子排布式是 。
其最高正价氧化物对应的水化物的化学式是 和 。
(2)元素X与Y形成的化合物晶体类型是 晶体
1mol该化合物含有的化学键数为 (用阿伏加德罗常数NA表示)
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是 ,该化合物中X原子的杂化轨道类型是 。
(4)X与碳、氢三种元素形成的相对分子质量最小的分子里有 个δ键, 个л键
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且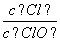 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
A.若某温度下,反应后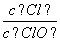 =11,则溶液中
=11,则溶液中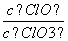 =
=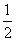
B.参加反应的氯气的物质的量等于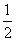 a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围: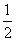 a mol≤ne≤
a mol≤ne≤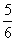 a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为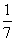 a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如右图:
反应物和产物的相关数据如下
| 相对分子质量 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成正丁醚的步骤:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g。
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为______________________________。
写出步骤②中制备正丁醚的化学方程式______________________________。
(2)加热A前,需先从__________(填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应从分液漏斗的  (填“上”或“下”)口分离出。
(填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为______________________________。
(5)步骤⑤中,加热蒸馏时应收集__________(填选项字母)左右的馏分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为__________,下层液体的主要成分为__________。(填物质名称)
(7)本实验中,正丁醚的产率为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com