
| A. | 中和滴定达中点时俯视滴定管内液面度数 | |
| B. | 碱式滴定管用蒸馏水洗净后立即装待测溶液来滴定 | |
| C. | 酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 | |
| D. | 把配好的标准溶液倒入刚用蒸馏水洗净的锥形瓶中然后用来滴定 |
分析 根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,若不消耗标准液体积偏大,则测定结果偏高,否则偏低,据此进行解答.
解答 解:A.中和滴定达中点时俯视滴定管内液面读数,导致读出的标准液体积偏大,计算出的标准液体积偏小,测定结果偏低,故A错误;
B.碱式滴定管用蒸馏水洗净后立即装待测溶液来滴定,导致标准液被稀释,滴定过程中消耗的标准液体积偏小,测定结果偏低,故B错误;
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定,导致标准液被稀释,滴定过程中消耗标准液体积偏大,测定结果偏高,故C正确;
D.把配好的标准溶液倒入刚用蒸馏水洗净的锥形瓶中然后用来滴定,导致锥形瓶中氢氧化钠的物质的量偏大,测定结果偏高,故D正确;
故选CD.
点评 本题主要考查了化学实验操作中的误差分析,题目难度中等,掌握中和滴定操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
 甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
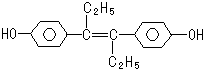
| A. | 它易溶于有机溶剂 | |
| B. | 该有机物可与少量Na2CO3反应放出CO2气体 | |
| C. | 1mol该有机物可以与5mol Br2发生反应 | |
| D. | 该有机物分子中,可能有16个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | B. | 20Ne和22Ne的质子数为10 | ||
| C. | 20Ne和22Ne的电子数相同 | D. | 20Ne和22Ne的中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 将甲的溶液从t2℃降到t1℃,其溶质的质量分数一定减小 | |
| B. | t2℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等 | |
| C. | 当温度高于0℃而低于t1℃时,乙的溶解度比甲的溶解度大 | |
| D. | t2℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉遇碘化钾溶液变蓝 | |
| B. | 葡萄糖和果糖互为同分异构体 | |
| C. | 利用油脂在碱性条件下水解可制取肥皂 | |
| D. | 用灼烧并闻气味的方法鉴别羊毛织物和棉织物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com