
【题目】消毒是饮用水处理中的重要环节之一。目前,常用的消毒剂有氯气、二氧化氯等。研究人员发现:1.0 mg/L氯气与0.5 mg/L二氧化氯的消毒能力相当,氯气和二氧化氯消毒过程中都会产生三氯甲烷(有毒副产物)。在40℃时,对两种消毒剂的浓度与产生三氯甲烷的浓度关系进行了对比实验。得出的数据如图1和图2所示。

![]()
下列说法不正确的是
A. 对比图1和图2可得出,浓度均为0.3 mg/L时,二者的消毒能力相当
B. 40℃时,4.0 mg/L的氯气在0~20 h内产生的三氯甲烷明显增多
C. 实验数据能表明,氯气和二氧化氯在消毒能力相当的情况下,使用二氧化氯做消毒剂比用氯气更安全。
D. 自来水厂以亚氯酸钠(NaClO2)和盐酸为原料,用二氧化氯发生器现场制二氧化氯的方程式为:5NaClO2 + 4HCl = 4ClO2 +5NaCl + 2H2O
【答案】A
【解析】根据题目表述“1.0 mg/L氯气与0.5 mg/L二氧化氯的消毒能力相当”,所以与图中表示无关,选项A错误。由图1得到4.0 mg/L的氯气在0~2h间曲线的斜率较大,说明三氯甲烷的量增加得很快,选项B正确。1.0 mg/L氯气与0.5 mg/L二氧化氯的消毒能力相当,对比两个图中的1.0 mg/L氯气与0.5 mg/L二氧化氯的曲线,得到氯气产生的三氯甲烷明显比二氧化氯产生的三氯甲烷多,所以使用二氧化氯更安全,选项C正确。亚氯酸钠与盐酸反应制取二氧化氯,Na元素在反应后明显只能以氯化钠的形式存在,根据化合价变化一定最小的基本原则,认为反应是亚氯酸钠的歧化反应,其中+3价的氯一部分升高到二氧化氯的+4价,一部分降低到氯化钠的-1价,所以应该有4个升高到二氧化氯,一个降低为氯化钠,所以配平得到:5NaClO2 + 4HCl = 4ClO2 +5NaCl + 2H2O。选项D正确。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.氧化物:CO2 NO SO2 H2O
B.碱:NaOH KOH Ba(OH)2 Na2CO3
C.铵盐:NH4Cl NH4NO3 (NH4)2SO4 NH3H2O
D.碱性氧化物:Na2O CaO Mn2O7 MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下: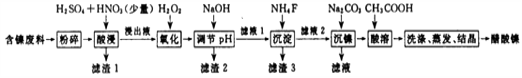
相关离子生成氢氧化物的pH和相关物质的溶解性如下表: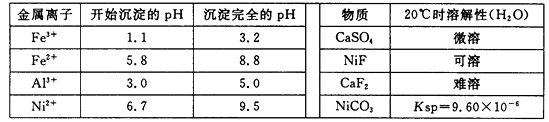
(1)调节pH步骤中,溶液pH的调节范围是。
(2)滤渣1和滤渣3主要成分的化学式分别是、。
(3)酸浸过程中,1mol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式。
(4)沉镍前c(Ni2+)=2.0 mol· L-1 , 欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],则需要加入Na2CO3固体的质量最少为g。(保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,两个恒容密闭容器中分别发生下列两个反应:①H2(g)+I2(g) ![]() 2HI(g) ②C(s)+H2O(g)
2HI(g) ②C(s)+H2O(g) ![]() CO(g)+H2(g),下列状态能表明两反应都达到平衡状态的是( )
CO(g)+H2(g),下列状态能表明两反应都达到平衡状态的是( )
a.各物质的浓度不变
b.容器内气体压强不变
c.容器内气体密度不变
d.容器内气体颜色不变
e.各组分的物质的量分数或质量分数不变
A.abc
B.ade
C.ac
D.ae
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
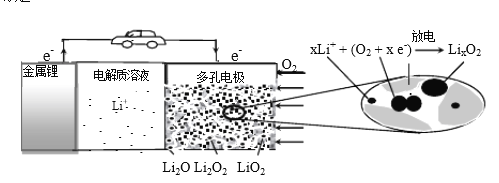
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(g) ![]() pC(g)达到平衡后,升高温度,B的转化率变大;当减小压强,C的体积分数减小。
pC(g)达到平衡后,升高温度,B的转化率变大;当减小压强,C的体积分数减小。
(1)用“>”、“=”或“<”填空:该反应的ΔH______0,m+n______p。
(2)用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入B,则A的转化率________;升高温度,则平衡时B、C的浓度之比c(B)/c(C)将________;加入催化剂,平衡时气体混合物的总物质的量________。
(3)若A、C均为无色气体,B为红色气体,用“变深”、“变浅”或“不变”填空:恒容下加入C,平衡混合物的颜色________;而恒压充入氖气,平衡混合物颜色________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com