
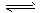 2NH3 (g)
2NH3 (g)  学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
| N2(g)+3H2(g)?2NH3(g) | |||
| N2 | H2 | NH3 | |
| 起始浓度mol/L | 1.0 | 3.0 | 0.2 |
| 2s末浓度mol/L | 0.6 | 1.8 | 1.0 |
| 4s末浓度mol/L | 0.4 | 1.2 | 1.4 |
| A、2s末氨气的反应速率为0.4mol/(L?s) |
| B、前2s时间内氨气的平均反应速率为0.4mol/(L?s) |
| C、前4s时间内氨气的平均反应速率为0.3mol/(L?s) |
| D、2s~4s时间内氨气的平均反应速率为0.2mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源:上海市十三校2011届高三12月联考化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
新华网2月22日电 截至22日15时,山西屯兰煤矿事故已造成73人遇难。据事故抢险指挥部介绍,现已初步查明,事故原因为井下局部瓦斯爆炸。该矿发生事故时井下共有矿工436人,有375人陆续升井。升井后经抢救无效死亡的和井下已发现遇难遗体的矿工共计73人。现有113人住院观察,其中21人伤势较重。目前,山西仍在全力搜救被困者,第一轮搜救已于14时结束,目前第二轮搜救排查已经展开,同时山西省还采取措施防止次生灾害发生。煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷。
![]() ⑴下列关于甲烷的叙述中错误的是( )
⑴下列关于甲烷的叙述中错误的是( )
![]() A.甲烷分子是一种呈正四面体型的、含极性键的非极性分子
A.甲烷分子是一种呈正四面体型的、含极性键的非极性分子
![]() B.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子
B.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子
![]() C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业
C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业
![]() D.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸
D.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸
![]() ⑵已知某正四面体形分子E和直线形分子G在光照条件下反应,生成一种直线形分子M和变形的四面体L(组成E.G.L.M分子的元素原子序数均小于18),且G分子中的原子处于E分子最大原子的下一周期。反应过程图示如下:
⑵已知某正四面体形分子E和直线形分子G在光照条件下反应,生成一种直线形分子M和变形的四面体L(组成E.G.L.M分子的元素原子序数均小于18),且G分子中的原子处于E分子最大原子的下一周期。反应过程图示如下:
![]()
![]() 利用E与G发生取代反应制取副产品M溶液的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:
利用E与G发生取代反应制取副产品M溶液的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:
![]()
![]()

根据要求填空:
![]() ①B装置有三种功能:①控制气流速度;②均匀混合气体;③
①B装置有三种功能:①控制气流速度;②均匀混合气体;③
![]() ②设V(G)/V(E)=x,若理论上欲获得最多的M,则x值应
②设V(G)/V(E)=x,若理论上欲获得最多的M,则x值应
![]() ③D装置的石棉中均匀混有KI粉末,其作用是 。
③D装置的石棉中均匀混有KI粉末,其作用是 。
![]() ④E装置的作用是 (填编号)
④E装置的作用是 (填编号)
![]() A.收集气体 B.吸收G物质 C.防止倒吸 D.吸收M物质
A.收集气体 B.吸收G物质 C.防止倒吸 D.吸收M物质
![]() ⑤在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式 。
⑤在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式 。
![]() ⑥E装置出生成盐酸外,还含有有机物,从E中分离出M的最佳方法为 。
⑥E装置出生成盐酸外,还含有有机物,从E中分离出M的最佳方法为 。
![]() 该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为
该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省高三12月月考理综考化学试卷(解析版) 题型:填空题
I.已知:反应H2(g) + Cl2(g) = 2HCl(g) ΔH= —184 kJ/mol
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol
2Cl2(g)+2H2O(g)
ΔH= —115.6 kJ/mol


请回答:
(1)H2与O2反应生成气态水的热化学方程式
(2)断开1 mol H—O 键所需能量约为 kJ
II.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: ,它所对应的化学方程式为:
,它所对应的化学方程式为:
(2)已知在400℃时,N2 (g)+ 3H2(g)
 2NH3(g)
△H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
2NH3(g)
△H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是 (填序号)(1分)
A.缩小体积增大压强 B.升高温度 C.加催化剂 D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:A(g) + 3B(g)  2C(g)
+ D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
2C(g)
+ D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
|
t/K |
300 |
400 |
500 |
… |
|
K/(mol·L—1)2 |
4×106 |
8×107 |
K1 |
… |
请完成下列问题:
①判断该反应的ΔH 0(填“>”或“<”) (1分)
②在一定条件下,能判断该反应一定达化学平衡状态的是 (填序号)
A.3v(B)(正)=2v(C)(逆) B.A和B的转化率相等
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)以天然气(假设杂质不参与反应)为原料的燃料电池示意图如图所示。

①放电时,负极的电极反应式为
②假设装置中盛装100.0 mL 3.0 mol·L—1 KOH溶液,放电时参与反应的氧气在标准状况下体积为8 960 mL。放电完毕后,电解质溶液中各离子浓度的大小关系为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com