
| A. | 2,4,5,6 | B. | 3,4,5,6 | C. | 2,3,4,5 | D. | 4,5,6,7 |
分析 由题给信息可知CH2═C(CH3)CH3与CH2═CHCH3发生烯烃复分解反应生成的烯烃有CH2═CH2、CH3C(CH3)═C(CH3)CH3、CH3C(CH3)═CHCH2CH3和CH3CH2CH═CHCH2CH3四种,与C=C直接相连的原子在同一个平面上,以此解答该题.
解答 解:因烯烃在合适催化剂作用下可双键断裂,两端基团重新组合为新的烯烃,则CH2═C(CH3)CH2CH3与CH2═CHCH2CH3发生烯烃复分解反应生成的烯烃有CH2═CH2、CH3CH2C(CH3)═C(CH3)CH2CH3、CH3CH2C(CH3)═CHCH2CH3和CH3CH2CH═CHCH2CH3四种,根据CH2═CH2分子的平面结构可知它们肯定在同一平面的碳原子数分别为:2个、6个、5个、4个.
故选A.
点评 本题考查有机物结构和性质,侧重考查学生获取信息利用信息解答问题能力,正确理解给予信息采用信息迁移的方法分析解答是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 实际应用 | 化学原因 | |
| A | “84”消毒液和洁厕灵不能混合使用 | 发生化学反应产生有毒气体 |
| B | FeCl3腐蚀Cu刻制印刷电路板 | 铁比铜金属性强 |
| C | 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 | 酸、碱还有盐可直接侵蚀铝的保护膜以及铝制品本身 |
| D | 明矾、硫酸铁可作净水剂 | 溶于水形成胶体从而凝聚水中的悬浮物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 豆科作物的根瘤菌对空气中氮的固定 | |
| B. | 将NO2气体冷却后颜色会变浅 | |
| C. | 熟石膏转化为生石膏 | |
| D. | 工业制液态氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 判定加热时有无晶体飞溅 | B. | 判断是否已失去全部结晶水 | ||
| C. | 判断是否有其他杂质 | D. | 防止失水后又吸潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4Cl受热易分解,可用作氮肥 | |
| C. | MgO熔点高,可用作耐高温材料 | |
| D. | KAl(SO4)2•12H2O易溶于水,可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
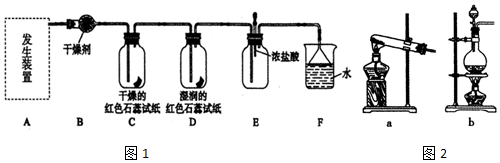
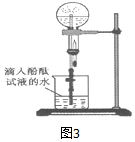
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 12g 12C含中子数为NA | |
| B. | 标准状况下,22.4L氖气中含有原子数为2NA | |
| C. | 28g CO和N2混合气体含有的原子数为2NA | |
| D. | 2mol钠与足量O2完全反应生成Na2O2时失去电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释或对应的离子方程式 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接和油污反应 |
| B | 酸雨样品在空气中放置pH减小 | 亚硫酸被氧化为硫酸 2H2SO3+O2=2H2SO4 |
| C | “84”消毒液具有漂白性 | ClO-+CO2+H2O=HClO+HCO3- |
| D | 用加热法除去NaCl固体中混有的NH4Cl固体 | NH4Cl固体可以完全分解成为气体而除去 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com