
下列离子在溶液中能大量共存的是( )
A.Cl-、NO、Fe3+、Na+ B.Ag+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42- D.Cu2+、NH4+、Br-、OH-
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:2015-2016学年山西大学附属中学高一上期中化学试卷(解析版) 题型:填空题
某无色透明溶液中可能大量存在下列离子中的几种:Na+、Mg2+、Ca2+、Fe2+、Cu2+、OH-、Cl-、CO32-、HCO3-、NO、SO42-。请填写下列空白:
(1)不做任何实验就可以肯定溶液中不存在的离子是 ;
(2)取少量原溶液滴加几滴酚酞试液,溶液变红色。此实验现象可说明原溶液中肯定不存在的离子是 ;
(3)另取少量原溶液逐滴滴加盐酸至过量,无气体、无沉淀生成,再加入BaCl2溶液后,有白色沉淀生成。此实验现象可说明原溶液中肯定不存在的离子还有 ;
(4)将(3)实验所得混合液静置,取少许上层清液并加入AgNO3溶液,有白色沉淀生成。
根据上述实验推断:原溶液中肯定存在的离子有______________,不能肯定存在的离子有___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某高校研究课题组利用生物发酵技术生产灵芝酸单体的分子结构图如右图所示,下列关于该有机物的说法不正确的是
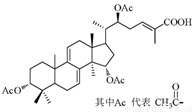
A.能与Br2发生加成反应
B.能发生酯化反应
C.能发生水解反应
D.分子中有7 个手性碳原子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东枣庄三中高二10月学情调查化学卷(解析版) 题型:选择题
如图所示,装置中都盛有0.1mol·L-1 的NaCl 溶液,放置一定时间后,装置中的四块相同的锌片腐蚀速率由快到慢的正确顺序是:( )
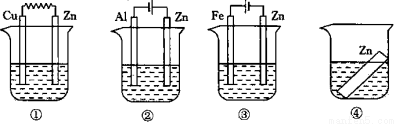
A.①②③④ B.①②④③ C.②①④③ D.③①④②
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东枣庄八中南校区高二12月月考化学卷(解析版) 题型:选择题
氨水中有下列平衡NH3•H2O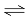 NH4++OH﹣,当其他条件不变时,改变下列条件,平衡向左移动,且NH4+浓度增大的是( )
NH4++OH﹣,当其他条件不变时,改变下列条件,平衡向左移动,且NH4+浓度增大的是( )
A.加NaOH 固体 B.加浓HCl
C.加NH4Cl固体 D.加同浓度的氨水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南南阳第一中学高一上第二次月考化学卷(解析版) 题型:选择题
下图中“—”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙,下面四组选项中,符合图示要求的是()
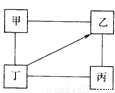
甲 | 乙 | 丙 | 丁 | |
A. | H2SO4 | Na2SO4 | NaOH | NaCl |
B. | KCl | K2CO3 | KOH | HCl |
C. | O2 | CO2 | CuO | C |
D. | Fe | CuCl2 | Zn | HCl |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北冀州市高一上第四次月考化学试卷(解析版) 题型:选择题
在强酸性溶液中能大量共存,且溶液为无色透明的离子组( )
A.K+、Na+、AlO2-、NO3- B.NH4+、Al3+、NO3-、SO42-
C.K+、NH4+、CO32-、S2- D.K+、Ag+、NO3-、MnO4-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上期中测试化学试卷(解析版) 题型:实验题
实验室需要配制0.50 mol/L NaCl溶液480 mL,现使用NaCl固体配制,按下列操作步骤填上适当的文字,以使整个操作完整。
Ⅰ.(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、__________、_________________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________ g。
(3)称量。
①天平调平。 ②称量。 ③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是___________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_______________________。
(6)定容、摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶中,并贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会______(填“偏高”、“偏低”或“无影响”)。
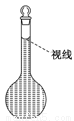
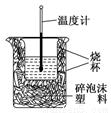
Ⅱ.实验室利用如图装置进行中和热的测定,请回答下列问题:
(1)该图中有两处未画出,它们是________________,________________。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_________________。
(3)如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将________(填“偏大”、“偏小”、“不变”);原因是_______________。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三12月月考化学试卷(解析版) 题型:选择题
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。用湿润的淀粉碘化钾试纸检验气体时,试纸先变蓝后褪色。下列有关说法正确的是( )
A.由反应可确定:氧化性HClO4 >HClO3
B.该反应的还原产物是O2和HClO4
C、试纸先变蓝后褪色是因为Cl2具漂白性
D.若化学计量数a=8,b=3,则该反应转移电子数为20e-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com