
全球海水中的溴的藏量丰富,约占地球溴的总藏量的99%,故溴有“海洋元素”之称。海水中溴含量为65mg/L。其工业提取方法有:
(1)空气吹出纯碱吸收法.方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及到的反应有:
①________________写出离子方程式);
②Br2+3CO32-=BrO3-+5Br-+3CO2↑;
③BrO3-+5Br-+6H+=3Br2+3H2O。
其中反应②中的氧化剂是___________;还原剂是_________;
(2)空气吹出SO2吸收法.该方法基本同(1),只是将溴吹出后是用SO2来吸收的,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴.写出溴与二氧化硫反应的化学方程式:___________;
(3)溶剂萃取法.该法是利用单质溴在水中和溶剂中溶解度的不同的原理来进行的.实验室中萃取用到的实验仪器名称是_________;下列可以用于海水中溴的萃取试剂的是_______;
①乙醇 ②四氯化碳 ③硝酸 ④裂化汽油
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届湖南省长沙市高三上学期月考化学试卷(解析版) 题型:选择题
将SO2通入CuSO4和NaCl的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀分析,知其中含Cl:35.7%,Cu:64.3%,SO2在上述反应中作用是
A.催化剂 B.漂白剂 C.还原剂 D.氧化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上期中测试化学试卷(解析版) 题型:选择题
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下进行反应,一段时间后测得反应前后各物质质量如表.该密闭容器中发生化学反应的基本类型可能是
物质 | X | Y | Z | Q |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 16 | 14 |
A.分解反应 B.置换反应 C.复分解反应 D.化合反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期中(文)化学试卷(解析版) 题型:选择题
日常生活和工业生产中常用到漂白剂,下列物质的溶液具有漂白作用的是
A.CuSO4 B.CaCl2 C.Na2SO4 D.Ca(ClO)2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
现有等体积,等物质的量浓度的NaCl、MgCl2、AlCl3三种溶液,用物质的量浓度相同的AgNO3溶液分别完全沉淀三种溶液中的Cl-。所消耗AgNO3溶液的体积比为
A.6∶3∶2 B.3∶2∶1 C.1∶2∶3 D. 1∶1∶1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一上12月段考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.CaCO3与盐酸反应:CO32-+2H+=CO2↑+H2O
B.铁与硫酸反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化铜与盐酸反应:H++OH-=H2O
D.锌与硫酸铜溶液反应:Zn+Cu2+=Zn2++Cu
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:选择题
甲乙两烧杯中分别盛有100mL、1mol/L的硫酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=5:6,则加入铝粉的质量为
A.2.16g B.1.08g C.2.7g D.5.4g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一12月月考化学试卷(解析版) 题型:选择题
等体积的AlCl3和NaOH两溶液混合,充分反应后,沉淀和溶液中所含铝元素的质量相等,则原AlCl3溶液和NaOH溶液物质的量浓度之比可能是
A.1:3 B.2:5 C.1:4 D.2:7
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期第五次月考化学试卷(解析版) 题型:填空题
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下反应:
(CH3)2NNH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g) (I)
(1)反应(I)中氧化剂是__________。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g) 2NO2 (g)(II)当温度升高时,气体颜色变深,则反应(II)为________(填“吸热”或“放热”)反应。
2NO2 (g)(II)当温度升高时,气体颜色变深,则反应(II)为________(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1molN2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是_______;
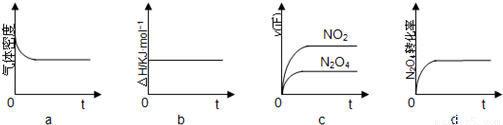
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)= ______mol•L-1•s-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com