
| 选项 | 实验 | 实验现象 | 实验结论 |
| A | 取少量食盐溶于水,加稀硫酸酸化再滴入淀粉溶液 | 溶液呈蓝色 | 食盐为加碘食盐 |
| B | 取两支试管,都加入2mL0.01mol/L的酸性KMnO4溶液,向其中一支试管加入2mL蒸馏水后,再同时向两支试管各加入2mL0.1mol/L的H2C2O4溶液 | 两试管中溶液紫色均褪去,且后者所用时间更短 | 酸性KMnO4溶液浓度越大,化学反应速率越快 |
| C | 向蛋白质溶液中加入CuCl2或 (NH4)2SO4饱和溶液 | 均有沉淀 | 蛋白质均发生了变性 |
| D | 将0.1mol/L MgSO4溶液滴入NaOH稀溶液至不再有沉淀产生,再滴加0.1mol/L CuSO4溶液 | 白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碘单质遇淀粉试液变蓝色;
B.反应物浓度越大反应速率越快;
C.铵盐能使蛋白质发生盐析,重金属盐能使蛋白质发生变性;
D.溶度积常数大的物质能转化为溶度积常数小的物质.
解答 解:A.碘单质遇淀粉试液变蓝色,碘酸钾中不含碘单质,所以与淀粉实验不反应变色,故A错误;
B.反应物浓度越大反应速率越快,溶液褪色时间越短,两试管中溶液紫色均褪去,且后者所用时间更短,因为后者中溶液体积变大,导致高锰酸钾和草酸浓度降低,反应速率减慢,所以后者褪色时间长,故B错误;
C.硫酸铵能使蛋白质发生盐析,但氯化铜能使蛋白质发生变性,二者原理不同,故C错误;
D.将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,说明NaOH完全反应,再滴加0.1mol•L-1CuSO4溶液,先有白色沉淀生成后变为浅蓝色沉淀,说明发生了沉淀的转化,溶度积大的物质向溶度积小的物质转化,所以Cu(OH)2的溶度积比Mg(OH)2的小,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及难溶物的转化、浓度对化学反应速率的影响、蛋白质的性质、碘的检验等知识点,明确实验原理及物质性质是解本题关键,注意蛋白质盐析和变性的区别,题目难度不大.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 变性蛋白质不能食用 | |
| B. | 可用甲醛浸泡海鲜 | |
| C. | SO2可以用来增白食品 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.
第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.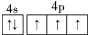 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
| A. | Z、Q均为ⅣA族元素 | |
| B. | X、Y、M三种元素中金属性最强的是M | |
| C. | R、Z形成的R2Z分子是非极性分子 | |
| D. | M的氢氧化物和Y的氢氧化物都能与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X与Y组成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | W、R两种元素对应的简单离子都能影响水的电离平衡 | |
| C. | 由X、Y、Z三种元素组成的化合物,其水溶液显碱性 | |
| D. | 工业上用电解熔融的Z和X组成的化合物来制取Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2 $\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$2CH3CHO+H2O | |
| C. | CH3CH2OH+CH3COOH $\stackrel{浓硫酸}{→}$CH3COOCH2CH3 | |
| D. | H2C═CH2+Br2→CH3CHBr2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com