
 +3HNO3 $→_{△}^{浓硫酸}$
+3HNO3 $→_{△}^{浓硫酸}$ +3H2O;
+3H2O; 分析 (1)乙烯和水发生加成反应生成乙醇;
(2)甲苯与浓硝酸发生取代反应生成2,4,6-三硝基甲苯;
(3)溴乙烷与NaOH的乙醇溶液共热发生消去反应生成乙烯和溴化钠和水;
(4)溴乙烷与NaOH溶液共热发生取代反应生成乙醇和溴化钠;
(5)1,3丁二烯和溴水1,4加成生成CH2Br-CH=CH-CH2Br.
解答 解:(1)乙烯和水发生加成反应生成乙醇,方程式:CH2=CH2 +H2O$→_{△}^{催化剂}$CH3CH2OH,
故答案为:CH2=CH2 +H2O$→_{△}^{催化剂}$CH3CH2OH;
(2)甲苯与浓硝酸发生取代反应生成2,4,6-三硝基甲苯,方程式: +3HNO3 $→_{△}^{浓硫酸}$
+3HNO3 $→_{△}^{浓硫酸}$ +3H2O,
+3H2O,
故答案为: +3HNO3 $→_{△}^{浓硫酸}$
+3HNO3 $→_{△}^{浓硫酸}$ +3H2O;
+3H2O;
(3)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯,溴乙烷与氢氧化钠乙醇溶液加热反应方程式:CH3CH2Br+NaOH $→_{△}^{醇}$CH2=CH2↑+NaBr+H2O,
故答案为:CH3CH2Br+NaOH $→_{△}^{醇}$CH2=CH2↑+NaBr+H2O;
(4)溴乙烷与NaOH溶液共热发生取代反应生成乙醇和溴化钠方程式:CH3CH2Br+NaOH→CH3CH2OH+NaBr;
故答案为:CH3CH2Br+NaOH→CH3CH2OH+NaBr;
(5)1,4加成发生CH2=CH-CH=CH2+Br2→CH2Br-CH=CH-CH2Br,
故答案为:CH2=CH-CH=CH2+Br2→CH2Br-CH=CH-CH2Br.
点评 本题考查有机化学反应方程式的书写,为高频考点,把握物质的性质及发生的化学反应为解答的关键,注意有机反应的条件,题目难度不大.


科目:高中化学 来源:2017届重庆一中高三上学期第二次月考化学试卷(解析版) 题型:选择题
某羧酸酯的分子式为C57H104O6,1 mol该酯完全水解可得到3 mol羧酸M和1 mol甘油[HOCH2CH(OH)CH2OH]。羧酸M的分子式为( )
A.C17H32O2 B.C18H34O2 C.C18H36O2 D.C19H36O2
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4NH3+5O2═4NO+6H2O | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3═Na2CO3+H2O+CO2 | D. | Cl2+2NaBr═2NaCl+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及其离子方程式 | 评 价 |
| A | 向沸腾的蒸馏水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O=Fe(OH)3↓+3H+ | 正 确 |
| B | 大理石溶于醋酸的反应:CaCO3+2H+=Ca2++CO2↑+H2O | 错误,醋酸应写为分子形式CH3COOH,CaCO3应写成离子形式 |
| C | 铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ | 错误,产物不符合客观事实 |
| D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
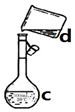 (1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图
(1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com