
【题目】对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g) ΔH<0。下列结论中错误( )
pC(g)+qD(g) ΔH<0。下列结论中错误( )
A. 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B. 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C. 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a
D. 若A为固体,则增大压强,平衡向逆向移动
【答案】D
【解析】
A、将容器的体积缩小到原来的一半,若平衡不移动,此时A的浓度变为原来的2倍,现在A的浓度为原来的2.1倍,说明平衡向着生成A的方向移动了;
B、当反应物的物质的量之比等于系数值比时,则达到化学平衡时,反应物的转化率是相等的;
C、对于反应前气体体积不变,混合气体总的物质的量不变;
D、对于反应前后气体体积不变的反应,压强不会影响平衡移动。
A、将容器的体积缩小到原来的一半,不考虑平衡移动,此时A的浓度变为原来的2倍,现在A的浓度为原来的2.1倍,说明平衡向着生成A的方向移动了,体积缩小即增大压强,平衡向着气体体积减小的方向进行,所以m+n<p+q,A正确;
B、反应开始时,A、B的物质的量之比为m∶n,恰好等于方程式的系数值比,这种情况下平衡时,A、B的转化率相等,B正确;
C、往含有amol气体的平衡体系中再加入amol的B,平衡向正反应移动,因为m+n=p+q,达到新平衡时混合气体总的物质的量不变,达到新平衡时气体的总物质的量等于2amol,C正确;
D、若A为固体,若n>p+q,则增大压强,平衡向正向移动;若n=p+q, 则增大压强,平衡向不移动;若n<p+q, 则增大压强,平衡向逆向移动;D错误;
综上所述,本题选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已经298K、101kPa时,下列说法不正确的是
反应1:4Fe(s)+3O2(g) = 2Fe2O3 (s) ΔH1 =-1648 kJ/mol
反应2:C(s) + O2 (g) = CO2 (g) ΔH2 = -393 kJ/mol
反应3:2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ΔH3 =-1480 kJ/mol
反应4:2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ΔH4
A. 上述反应1.2.3.4在热力学上自发趋势都很大
B. 反应1和3在较低温度下能自发反应,反应4是熵增反应
C. 自发反应代表反应一定能发生,可以判断过程的方向,但不能确定过程发生的速率
D. 反应1表示铁在氧气中燃烧的热化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池已用于航天飞机,其工作原理如图所示。关于该燃料电池的说法不正确的是
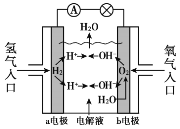
A. H2在负极发生氧化反应
B. 电子从a电极经外电路流向b电极
C. 供电时的总反应为:2H2 + O2 == 2H2O
D. 燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO3-离子中的两种组成的溶液,可以发生如图转化,下列说法正确的是

A. 甲为HCl,乙为NaHCO3
B. 溶液丙中还可以大量共存的离子有:Fe2+、NO3-、SO42-
C. 在甲中滴加丁开始反应的离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O
D. 白色沉淀A可能溶解在溶液D中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.5mol N2O4气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时,NO2的浓度为0.02 mol/L。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是( )
A. 前2秒,以N2O4的浓度变化表示的平均反应速率为0.01mol/(L·s)
B. 在2秒时体系内的压强为开始时的1.2倍
C. 在平衡时体系内含N2O40.20mol
D. 平衡时,如果再充入一定量N2O4, 则可提高N2O4的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关除杂质(括号中为杂质)的试剂及操作中,不正确的是
A.乙烷(乙烯):溴水,洗气B.乙醇(水):蒸馏
C.乙酸乙酯(乙酸):饱和碳酸钠溶液,分液D.溴苯(溴):氢氧化钠溶液,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的分子式为____________。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行如下实验,研究化学反应中的热量变化。
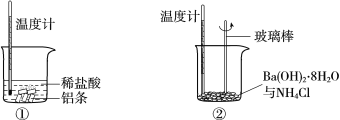
请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________反应(填“放热”或“吸热”,下同),Ba(OH)2·8H2O与NH4Cl的反应是________反应。
(2)①中反应的离子方程式是_________,该反应的还原剂是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com