
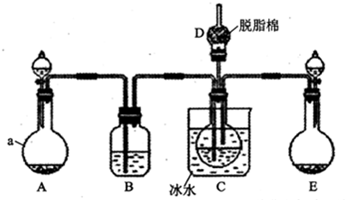

���� ��1�����ݳ��õ��������ƽ��
��2��Bװ�õ�����Ϊ��ȥ������̼�е��Ȼ��⣬������̼�ڱ���̼��������Һ���ܽ�Ȳ����Ȼ����ܹ���̼�����Ʒ�Ӧ���ɶ�����̼��
��3�����ݶ�����̼�Ͱ������ܽ����ж���ͨ������壬������������ˮ�����ڶ�����̼�����գ�����Ӧ��ͨ�백����
��4�������ӷ�������Ϊ�������壬���ᷴӦ������Ӧ��Ũ�������ǿ�����ԣ�Ũ�����ӷ���
��5���ⶨC�����þ����̼�����ƵĴ��ȣ����辧���в���̼�������ʣ����������ָ����������Ϊwg����ʱΪ̼�����ƴ�Ʒ����������1��������ȵ��������ٱ仯ʱ�����÷�ĩΪ̼���ƺ����ʣ�Ȼ���ܽ⣬��������������Һ������������̼���Ʒ�Ӧ����̼�ᱵ�������ɵ�̼�ᱵ���ˡ�ϴ�ӡ��������Ϊn g�����ݹ�ϵʽ2NaHCO3--BaCO3�������̼�����Ƶ�������
��� �⣺��1��Aװ��Ϊ��ȡ������̼��װ�ã�����aΪԲ����ƿ���ʴ�Ϊ��Բ����ƿ��
��2��Bװ�õ�����Ϊ��ȥ������̼�е��Ȼ��⣬������̼�ڱ���̼��������Һ���ܽ�Ȳ����Ȼ����ܹ���̼�����Ʒ�Ӧ���ɶ�����̼������B��ʢ���Լ�Ϊ����̼��������Һ��
�ʴ�Ϊ���ߣ�
��3��CO2��ˮ���ܽ��С��������������ˮ������ͨNH3�����ͣ�Ȼ��ͨ�������̼���壬������NaHCO3������
�ʴ�Ϊ��NH3��CO2��ˮ���ܽ��С����ͨNH3�����ͣ�������NaHCO3������
��4�������ӷ���D����֬��Ӧ������Լ������ݳ��İ�����Ũ������ʹ����ˮ��Ũ������лӷ��ԣ�����Ϊ�������壬�����ᷴӦ������ѡ��ϡ���ᣬ
�ʴ�Ϊ��b��
��5���ⶨC�����þ����̼�����ƵĴ��ȣ����辧���в���̼�������ʣ����������ָ����������Ϊwg����ʱΪ̼�����ƴ�Ʒ����������1��������ȵ��������ٱ仯ʱ�����÷�ĩΪ̼���ƺ����ʣ�Ȼ���ܽ⣬��������������Һ������������̼���Ʒ�Ӧ����̼�ᱵ�������ɵ�̼�ᱵ���ˡ�ϴ�ӡ��������Ϊn g��
��Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O����Na2CO3+Ba��OH��2=BaCO3 ��+2NaOH���õ���̼�ᱵ��Ҫ�������ˡ�ϴ�ӡ�����ɳ�����
����Ʒ��̼�����Ƶ�����Ϊx��������ʽ�ɵù�ϵʽ��
2NaHCO3��BaCO3
84��2 197
x n
$\frac{84��2}{x}$=$\frac{197}{n}$��x=$\frac{168n}{197}$��
���þ�����̼�����ƵĴ���$\frac{168n}{197w}$��100%��
�ʴ�Ϊ�����ˣ�ϴ�ӣ����$\frac{168n}{197w}$��100%��
���� ���⿼���˹�ҵ�ƴ����ԭ�����������������е����ʱ仯�������ɷֵķ����жϺͼ���Ӧ�ã�ע��ʵ����̷��������Ӳ�����β�������ǽ��ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | b-m-n | B�� | b+m-n | C�� | b-m+n | D�� | b+m+n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | NaCl | MgCl2 | AlCl3 | SiCl4 | ����R |
| �۵� | 810�� | 710�� | 180�� | -70�� | 2300�� |
| �е� | 1465�� | 1418�� | 177.8�� | 57�� | 2500�� |
| A�� | SiCl4�Ƿ��Ӿ��� | |
| B�� | MgCl2�м���ǿ�ȱ�NaCl�м���ǿ��С | |
| C�� | ����R������ԭ�Ӿ��� | |
| D�� | AlCl3Ϊ���Ӿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
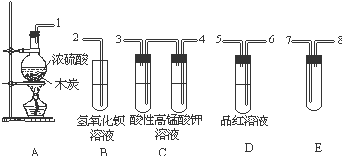 ŨH2SO4��̿��Ӧ������ɷֿ�����ͼװ����ȷ�ϣ�
ŨH2SO4��̿��Ӧ������ɷֿ�����ͼװ����ȷ�ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��ѧ�ĺ�����Ӧ�û�ѧԭ���Ի�����Ⱦ�������� | |
| B�� | �뵼����ҵ����һ�仰������ɳ̲���û����������оƬ�IJ����Ƕ������� | |
| C�� | PM 2.5��ָ������ֱ���ӽ�2.5��10-6m�Ŀ������ɢ�ڿ������γɽ��� | |
| D�� | ������Ч���ܡ�̫���ܵ����͵綯�������Խ�����л�����β���ŷ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ڿ�����ȼ�յĻ���ʻ�ɫ������Ϊ���ɵ�Na2O2Ϊ����ɫ���� | |
| B�� | ��˿��Cl2��ȼ���к���ɫ���̣�����Ϊ���ɵ�FeCl3Ϊ����ɫ���� | |
| C�� | ������������ϡHNO3����ַ�Ӧ����KSCN��Һ����Һ�ʺ�ɫ��˵��ϡHNO3��Fe����ΪFe3+ | |
| D�� | ȡ������ҺX�������м����������Ƶ���ˮ���ټӼ���KSCN��Һ����Һ��죬˵��X��Һ��һ������Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na������O2��ȼ�գ�����1mol O2ʱת�Ƶĵ�������4��6.02��1023 | |
| B�� | ��״���£�6.72L NO2��ˮ���ӳ�ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA | |
| C�� | ����ʹ���Ļ����ҺpH=1������Һ��c��H+��=0.1��mol/L | |
| D�� | 1��L��0.1��mol/L��NH4Cl��Һ�е�NH4+����0.1��6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 78gNa2O2�������������������Ӹ�����Ϊ2NA | |
| B�� | HBr�ĵ���ʽΪH+��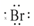 ��- ��- | |
| C�� | 3.4g�������0.6NA��N-H�� | |
| D�� | PCl3��BCl3����������ԭ�ӵ�����㶼�ﵽ8�����ȶ��ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶ȣ��淴Ӧ������������Ӧ���ʼ�С | |
| B�� | ����ʱ������ѹǿ��COŨ�Ȳ��� | |
| C�� | �÷�Ӧ�Ļ�ѧ����ʽΪ��CO2+H2?CO+H2O | |
| D�� | �÷�Ӧ���ʱ�Ϊ��ֵ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com