
分析 过氧化钠与二氧化碳、水反应均生成氧气,所以过氧化钠可用于呼吸面具和潜水艇中作为氧气的来源,原因是利用该反应可以将人体呼出的二氧化碳和水蒸气转化成人体需要的氧气,主要是呼出的二氧化碳和过氧化钠反应提供氧气.
解答 解:人体呼出的二氧化碳和水蒸气,过氧化钠与二氧化碳反应生成碳酸钠和氧气,与水反应生成氢氧化钠和氧气,化学方程式:2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑,主要是呼出的二氧化碳和过氧化钠反应提供氧气,
故答案为:2Na2O2+2CO2═2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑.
点评 本题考查了化学方程式的书写,题目难度不大,明确反应的实质是解题关键,注意钠的化合物过氧化钠的性质为高频考点.


科目:高中化学 来源: 题型:选择题
| A. | Na2C03溶液中:c(Na+)>c(C032-)>c(OH-)>c(HC03-)>c(H+) | |
| B. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COOH)+c(CH3C00-) | |
| C. | NaHC03溶液中:c(C032-)+c(OH-)=c(H+)+c(H2C03) | |
| D. | 氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔化状态下,能导电的物质一定是电解质 | |
| B. | 溶于水能导电的物质一定是电解质 | |
| C. | 熔化状态下,不能导电的化合物一定不是电解质 | |
| D. | BaSO4是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
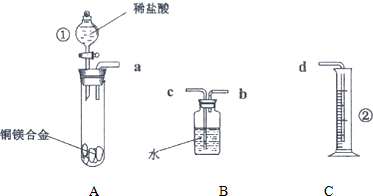
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH≡C-CH3 | B. | 对二甲苯 | C. | 对甲乙苯 | D. | 邻甲乙苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④②① | C. | ④①②③ | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向饱和食盐水中加入少量的浓盐酸,看不到明显的现象 | |
| B. | 将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀是以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小 | |
| C. | 在0.01mol/L NaCl溶液中加入少量的AgNO3溶液,有白色沉淀生成,接着向上述溶液中加入足量的浓氨水,白色沉淀不会溶解 | |
| D. | CaCO3溶液的导电能力很弱,是因为CaCO3是弱电解质,存在如下电离平衡:CaCO3?Ca2++CO${\;}_{3}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com