

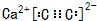 ,三键中含有2个π键、1个σ键,则π键和σ键数目之比为2:1,故答案为:
,三键中含有2个π键、1个σ键,则π键和σ键数目之比为2:1,故答案为: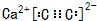 ;2:1;
;2:1;

科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:

| ① |
| ② |
| ③ |
| ④ |
| ⑤ |
| ⑥ |
| ⑦ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜片上有凹陷的“Cu”字 |
| B、铜片无任何变化 |
| C、发生了反应:Fe3++Cu=Cu2++Fe2+ |
| D、烧杯中的溶液呈棕黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgCl不溶于水,不能转化为AgI |
| B、一定温度下,向AgCl的饱和溶液中加入NaCl固体,有AgCl固体析出 |
| C、AgI比AgCl更难溶于水,所以AgCl可以转化为AgI |
| D、向AgCl沉淀的悬浊液中加入NaCl饱和溶液,AgCl的溶解度变小,溶度积常数变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m的值为2.56 |
| B、反应之前硝酸溶液的浓度为8 mol/L |
| C、NO与NO2混合气中NO与NO2的体积之比为1:5 |
| D、沉淀的最大质量为(m+0.8×17)g |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、F-结构示意图为: |
B、HCl的电子式为: |
C、Na2O2的形成过程可以表示为: |
| D、次氯酸(HClO)的结构式为:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔点:C>SiC>Si |
| B、沸点:NH3>AsH3>PH3 |
| C、熔点MgO>H2O>N2>O2 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com