
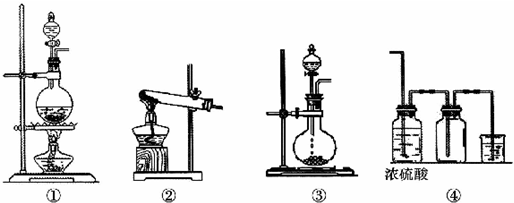
分析 (1)实验室如果用②装置制取氨气是固体和固体加热反应生成氨气,利用氯化铵和氢氧化钙加热反应生成;如果用浓氨水和氧化钙混合制取氨气是固体和液体不加热制备,据此选择装置,氨气是碱性气体遇到湿润的紫色石蕊试纸变蓝;
(2)收集气体的方法的选择可依据气体的密度和溶解性,如气体与氧气反应则只能用排水法收集;氧气的密度比空气大,难溶于水,可用排水法或向上排空气法收集;
(3)氯气有毒,不能直接排放到空气中,应有尾气吸收装置,NO不能用排空气法收集,氢气不能用向上排空气法收集,二氧化碳气体无需尾气吸收装置.
解答 解:(1)实验室如果用②装置制取氨气是固体和固体加热反应生成氨气,利用氯化铵和氢氧化钙加热反应生成,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3+2H2O+CaCl2,如果用浓氨水和氧化钙混合制取氨气是固体和液体不加热制备,据此选择装置③完成,检验氨气已收集满的方法是:将湿润的红色石蕊试纸靠近倒置的瓶口,如试纸变蓝,说明已满(或用蘸有浓盐酸的玻璃棒接近倒置的瓶口,如冒白烟,则表明氨气已满),
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3+2H2O+CaCl2;③;将湿润的红色石蕊试纸靠近倒置的瓶口,如试纸变蓝,说明已满(或用蘸有浓盐酸的玻璃棒接近倒置的瓶口,如冒白烟,则表明氨气已满);
(2)收集气体的方法的选择可依据气体的密度和溶解性,如气体与氧气反应则只能用排水法收集,气体是否有颜色与收集方法无关,与稳定性无关,氧气的密度比空气大,难溶于水,可用排水法或向上排空气法收集,用d装置收集氧气时应从长导管进入气体,b装置气体进入不能排出集气瓶的空气,
故答案为:②④;
(3)若用A装置与D装置相连制取收集X气体,是固体液体加热制备的气体,气体不能和浓硫酸发生反应,密度比空气重,可以用向上排气法收集,
①CO2 制备不需要加热,二氧化碳气体无需尾气吸收装置,故①错误;
②NO 可以制备但不能用排空气法收集,故②错误;
③Cl2 是固体和液体加热制备,用浓硫酸干燥,用向上排空气法收集,故③正确;
④H2 制备不需要加热,氢气比空气轻不能用向上排空气法收集,故④错误;
故答案为:③.
点评 本题考查气体的制备和收集、装置分析判断,注意从物质的性质角度选择制备方法和收集方法,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 升高温度(不考虑盐酸挥发) | B. | 改用10 mL 0.1 mol/L硝酸 | ||
| C. | 加入NaCl溶液 | D. | 滴入几滴硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | B. | Cu+2AgNO3=2Ag+Cu(NO3)2 | ||
| C. | CaO+H2O=Ca(OH)2 | D. | 3NaOH+FeCl3=3NaCl+Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.01mol/(L•s) | ||
| C. | v(B)=0.60 mol/(L•min) | D. | v(C)=1.00 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,将 4molSO2和2molO2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态 A 时,测得气体总物质的量为 4.2mol.若SO2、O2、SO3的起始物质的量分别用 a、b、c表示,回答下列问题:
如图所示,将 4molSO2和2molO2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态 A 时,测得气体总物质的量为 4.2mol.若SO2、O2、SO3的起始物质的量分别用 a、b、c表示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )
2011年,麻省理工学院科研团队研发出一种人造树叶,它将一片半导体材料夹在两层特殊的催化剂的中间.若将人造树叶整体浸泡在溶液中,当光照在人造树叶上,就会分解水生成H2和O2,结构如图所示.下列有关人造树叶说法正确的是( )| A. | 该装置最终将太阳能转变为电能 | |
| B. | Ni、Mo、Zn基催化剂极为阳极,发生氧化反应 | |
| C. | 可以将人造树叶浸泡在碱性溶液中 | |
| D. | 钴基催化剂上发生反应:2H2O-4e-=4H++O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | CH4O | C. | C2H4O | D. | C2H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .用1mol E合成1,4-二苯基丁烷,理论上需要消耗氢气4mol.
.用1mol E合成1,4-二苯基丁烷,理论上需要消耗氢气4mol. +CH2=CH2$\stackrel{AlCl_{3}/HCl}{→}$
+CH2=CH2$\stackrel{AlCl_{3}/HCl}{→}$ .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com