
依据事实,写出下列反应的热化学方程式。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为______________________________。
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的化学方程式为______________________________。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为________________________________。
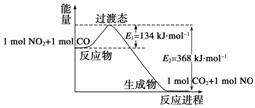
(4)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________________________。
(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g)
ΔH1=-867 kJ·mol-1①
2NO2(g)N2O4(g) ΔH2=-56.9 kJ·mol-1②
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式________。
答案 (1)N2(g)+2O2(g)===2NO2(g)
ΔH=+67.8 kJ·mol-1
(2)C6H12O6(s)+6O2(g)===6H2O(l)+6CO2(g)
ΔH=-2 804 kJ·mol-1
(3)SiH4(g)+2O2(g)===SiO2(s)+2H2O(l)
ΔH=-1 427.2 kJ·mol-1
(4)NO2(g)+CO(g)===CO2(g)+NO(g)
ΔH=-234 kJ·mol-1
(5)CH4(g)+N2O4(g)===N2(g)+CO2(g)+2H2O(g) ΔH=-810.1 kJ·mol-1
解析 (1)23 g NO2的物质的量为0.5 mol,则生成2 mol NO2吸收的热量为67.8 kJ。吸热反应ΔH为正值,故反应的热化学方程式为N2(g)+2O2(g)===2NO2(g) ΔH=+67.8 kJ·mol-1。(2)18 g葡萄糖的物质的量为0.1 mol,故1 mol葡萄糖燃烧生成CO2和液态水放出2 804 kJ的热量,反应的热化学方程式为C6H12O6(s)+6O2(g)===6H2O(l)+6CO2(g) ΔH=-2 804 kJ·mol-1。(3)2 g SiH4自燃放出热量89.2 kJ,1 mol SiH4自燃放出热量1 427.2 kJ,故热化学方程式为SiH4(g)+2O2(g)===SiO2(s)+2H2O(l) ΔH=-1 427.2 kJ·mol-1。(4)由图可知放出能量:ΔE=368 kJ·mol-1-134 kJ·mol-1=234 kJ·mol-1。(5)用①式-②式即可得目标方程式。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
①纯净的碳酸钠ag;②碳酸钠与碳酸氢钠的混合物a g,两者相比下列各种情况的描述正确的是( )
A.分别和盐酸完全反应时,混合物的耗酸量大
B.分别和盐酸完全反应时,纯净的碳酸钠放出CO2多
C.分别溶于水,再加入足量澄清石灰水,混合物得到的沉淀质量大
D.分别配成等体积溶液,混合物溶液中的Na+的物质的量浓度大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.NaCl溶液在电流的作用下电离成Na+和Cl-
B.溶于水后能电离出氢离子的化合物都是酸
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钡难溶于水,但硫酸钡属于强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
在微生物作用的条件下,NH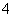 经过两步反应被氧化成NO
经过两步反应被氧化成NO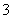 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
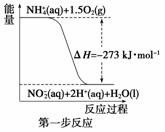
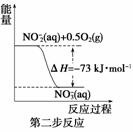
①第一步反应是________反应(选填“放热”或“吸热”),判断依据是________________________________________________________________________。
②1 mol NH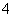 (aq)全部氧化成NO
(aq)全部氧化成NO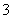 (aq)的热化学方程式是________________________________________________________________________。
(aq)的热化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,气态分子断开1 mol化学键的焓变称为键焓。已知H—H、H—O和O===O键的键焓ΔH分别为436 kJ·mol-1、463 kJ·mol-1、495 kJ·mol-1。下列热化学方程式正确的是( )
A.H2O(g)===H2(g)+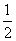 O2(g)
O2(g)
ΔH =-485 kJ·mol-1
B.H2O(g)===H2(g)+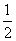 O2(g)
O2(g)
ΔH=+485 kJ·mol-1
C.2H2(g) + O2(g)===2H2O(g)
ΔH=+485 kJ·mol-1
D.2H2(g) + O2(g)===2H2O(g)
ΔH=-485 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)胆矾失水的热化学方程式为CuSO4·5H2O(s)===CuSO4(s)+5H2O(l)
ΔH=+Q1 kJ·mol-1
(2)室温下,无水硫酸铜溶于水的热化学方程式为
CuSO4(s)===Cu2+(aq)+SO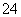 (aq)
(aq)
ΔH=-Q2 kJ·mol-1
(3)胆矾(CuSO4·5H2O)溶于水时溶液温度降低。
则Q1与Q2的关系是(Q1、Q2为正数)( )
A.Q1>Q2 B.Q1=Q2
C.Q1<Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
有NaCl、 FeCl2、、 FeCl3 、MgCl2、 AlCl3五种溶液,用一种试剂就可以将它们鉴别出来,这种试剂是 ( )
A.H2SO4 B.NaOH C.BaCl2 D.KSCN
查看答案和解析>>
科目:高中化学 来源: 题型:
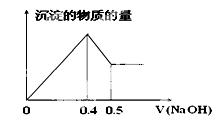
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液的体积关系如图所示,原溶液中Cl- 与SO42- 的物质的量之比为 ( )
A.1 :3 B.2 :3 C.6 :1 D.3 :1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某强酸性溶液中存在较多的Ba2+、NO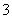 ,则该溶液中还可能大量存在的离子组是( )
,则该溶液中还可能大量存在的离子组是( )
A.K+、NH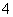 、HCO
、HCO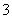 B.Fe2+、Ca2+、Cl-
B.Fe2+、Ca2+、Cl-
C.Cu2+、Mg2+、SO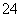 D.Na+、Cu2+、Cl-
D.Na+、Cu2+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com