
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | Fe2+ | 7.0 | 9.0 | Fe3+ | 1.9 | 3.2 | Cr3+ | 6.0 | 8.0 |


科目:高中化学 来源: 题型:阅读理解
| O | 2- 7 |
| 氢氧化物开始沉淀时的pH | 氢氧化物开始沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |
| O | 2- 7 |
| O | 2- 7 |
| O | 2- 7 |
| O | 2- 7 |
| O | 2- 7 |
| O | 2- 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |


查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省济宁市高三上学期期末阶段性教学质量检测化学试卷 题型:填空
(11分)欲降低废水中重金属元素铬的毒性,可将Cr2O2-7转化为Cr(OH)3沉淀除去。已知:

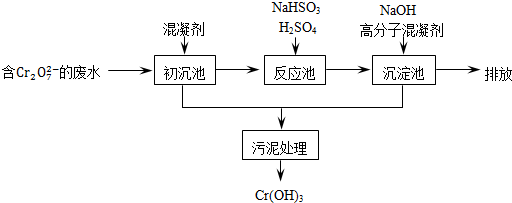
(1)某含铬废水处理的主要流程如图所示:
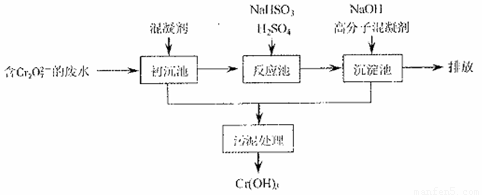
①沉池中加入的混凝剂是K2SO4·Al2(SO4)3·24H2O,用离子方程式表示其反应原理
。
②反应池中发生主要反应的离子方程式是Cr2O2—7+3HSO—3+5H+===2Cr3++3SO2—4+H2O。根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是 、 。证明Cr3+沉淀完全的方法是 。
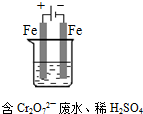
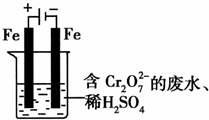
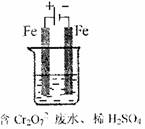
(2)工业亦可用电解法来处理含Cr2O2-7废水。实验室利用如图模拟处理含Cr2O2-7的废水,阳极反应式是Fe—2e—===Fe2+,阴极反应式是2H++2e—=H2↑。Fe2+与酸性溶液中的Cr2O2—7反应生成Cr3+和Fe3+,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是: 。
用电解法处理该溶液中0.01molCr2O2-7时,至少得到沉淀的质量是 g。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com