
| 坩埚质量(g) | 坩埚和晶体的总质量(g) | 加热后坩埚和剩余固体的质量(g) |
| 11.685 | 13.691 | 12.948 |
分析 (1)测定流程为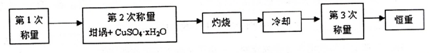 ,需要加热2次再测定质量,实验前测定坩埚的质量、坩埚和晶体的质量;
,需要加热2次再测定质量,实验前测定坩埚的质量、坩埚和晶体的质量;
(2)利用加热后两次测定的质量不变判断硫酸铜晶体加热时完全变成无水硫酸铜;
(3)由表格的数据可知,晶体的质量为13.691g-11.685g=2.006g,结晶水的质量为13.691g-12.948g=0.743g,结合CuSO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+xH2O计算;
(4)造成结果偏低,则不当操作导致水的质量测定偏小,以此来解答.
解答 解:(1)由 ,需要加热2次再测定质量,实验前测定坩埚的质量、坩埚和晶体的质量可知,本实验至少需要加热2次.至少需要称量4次,故答案为:2;4;
,需要加热2次再测定质量,实验前测定坩埚的质量、坩埚和晶体的质量可知,本实验至少需要加热2次.至少需要称量4次,故答案为:2;4;
(2)通过实验知道,要确保结果的准确性,本实验中的一个关键是通过恒重操作来判断硫酸铜晶体加热时是否完全变成无水硫酸铜,
故答案为:恒重操作;
(3)由表格的数据可知,晶体的质量为13.691g-11.685g=2.006g,结晶水的质量为13.691g-12.948g=0.743g,
CuSO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+xH2O
160+18x 18x
2.006g 0.743g
$\frac{160+18x}{2.006g}$=$\frac{18x}{0.743g}$,
解得x=5.23,
故答案为:5.23;
(4)a.加热前称量时坩埚未完全干燥,水的质量偏大,造成结果偏高,故不选;
b.加热过程中有少量晶体溅出,水的质量偏大,造成结果偏高,故不选
c.加热时坩埚内物质变黑,硫酸铜分解生成CuO,水的质量偏大,造成结果偏高,故不选;
d.加热后放在空气中冷却,水的质量偏小,造成结果偏低,故选;
e.最后两次加热后称量的质量差大于0.001g,结晶水没有完全失去,水的质量偏小,造成结果偏低,故选;
故答案为:de.
点评 本题考查物质含量的测定实验,为高频考点,把握测定原理、实验仪器的使用、实验技能等为解答的关键,侧重分析与实验能力的考查,注意结晶水含量的误差分析,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 主族元素的电负性越大,元素原子的第一电离能一定越大 | |
| B. | 在元素周期表中,元素电负性从左到右越来越小 | |
| C. | 在形成化合物时,电负性越小的元素越容易显正价 | |
| D. | 金属元素的电负性一定小于非金属元素的电负性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同族元素,随着核外电子层数的增加,I1逐渐增大 | |
| B. | 通常情况下,对于同一种元素的原子,其电离能I1<I2<I3 | |
| C. | 同周期元素,总体变化趋势是随着核电荷数的增加,I1增大 | |
| D. | 通常情况下,电离能越小,元素的金属性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
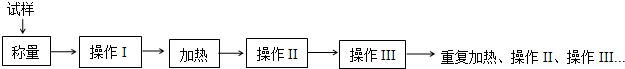
| 加热前质量 | 加热后质量 | ||
| m1 | m2 | m3 | m4 |
| 5.400g | 7.900g | 6.900g | 6.901g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
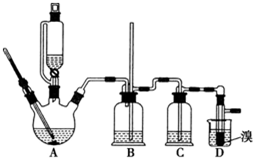 实验室制备 1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{1700℃}^{H_{2}SO_{4}(浓)}$CH2=CH
实验室制备 1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{1700℃}^{H_{2}SO_{4}(浓)}$CH2=CH| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量样品→加热→冷却→称量CuO | |
| B. | 称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 | |
| C. | 称量样品→加热→冷却→称量Cu(NO3)2 | |
| D. | 称量样品→加NaOH→过滤→加热→冷却→称量CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
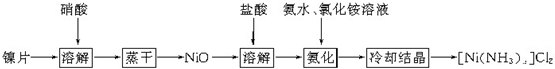
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com