
【题目】由以下一些微粒:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,其中:
,其中:
(1)互为同位素的是________和________;
(2)质量数相等,但不能互称同位素的是_________和__________;
(3)中子数相等,但质子数不相等的是______和_______、______和_______。
科目:高中化学 来源: 题型:
【题目】一些常见有机物的转化如图下列说法正确的是( )

A. 上述有机物中只有C6H12O6属于糖类物质 B. 物质A和B都属于电解质
C. 物质C和油脂类物质互为同系物 D. 转化1可在人体内完成,该催化剂属于蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为_________________。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,若将该反应原理设计成原电池,请写出原电池的正极反应______________________________。
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

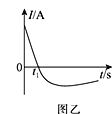
t1s前,原电池的负极是铝片,正极的电极反应式为________,溶液中的H+向______(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)H2(g)+CO2(g).在500℃时,平衡常数K=9.若反应开始时,一氧化碳和水蒸气的浓度都是0.02mol/L,则在此条件下CO的转化率为( )
A.25%
B.50%
C.75%
D.80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某处温泉有“圣水”之美誉,经常洗浴对治疗各种皮肤病、神经衰弱等有特殊的功效。经专家鉴定泉水中含有人体生命活动所需的微量元素,它们可能是
A.Fe、Mn、Zn、MgB.Zn、Cu、Mn、Ca
C.Zn、Cu、B、MnD.Mg、Mn、Cu、Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4HSO4溶液中,离子浓度由大到小的顺序正确的是
A. c(NH4+)>c(SO42-)>c(H+)>c(OH-) B. c(H+)>c(SO42-)> c(NH4+)> c(OH-)
C. c(SO42-)> c(NH4+)> c(H+)> c(OH-) D. c(SO42-)> c(NH4+)> c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组实验室制取乙酸乙酯时查阅资料如下:
主反应:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
副反应:2CH3CH2OH![]() CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
根据查得的资料设计了下图所示的装置(夹持装置忽略)制取纯净的乙酸乙酯。

步骤如下:
①在图1的三口烧瓶中加入3mL乙醇,边摇动边慢慢加入3mL浓硫酸,在分液漏斗中装入3:2的乙醇和乙酸混合液。
②油浴加热三口烧瓶至一定温度,然后把分液漏斗中的混合液慢慢地滴入三口烧瓶里并保持反应混合物在一定温度。
③反应一段时间后,向锥形瓶中缓慢加入饱和Na2CO3溶液,并不断摇动,分层后进行分液。
④用饱和食盐水和氯化钙溶液洗涤酯层,再分液,在酯层加入干燥剂干燥得粗乙酸乙酯。
⑤将粗乙酸乙酯转入图2的仪器A中,在水浴中加热,收集74~80℃的馏分即得纯净的水果香味无色透明液体。
根掲题目要求回答:
(1)在实验中浓硫酸的作用______;混合液加热前都要加入碎瓷片,作用是________。
(2)歩驟②中油浴加热保持的一定温度范围_____,原因是________。
(3)图2中仪器A的名称是_____,冷凝管中冷水从______(填a或b)口进入。
(4)步骤③和④中都用到了分液操作,该操作用到的主要玻璃仪器是_____,在分液操作时,上下两层液体移出的方法是____________。
(5)步骤④中干燥乙酸乙酯,可选用的干燥剂为______(填字母)。
a.五氧化二磷 b.无水Na2SO4 c.碱石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.
请回答下列问题:
(1)“O”点冰醋酸不能导电的原因是 .
(2)a、b、c三点对应的溶液中,C(H+)由小到大的顺序为 . (填字母,后同)
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是 .
(4)a、b、c三点对应的溶液中,水的电离程度最大的是 .
(5)若使c点对应的溶液中的c(CH3COO﹣)增大,在下列措施中,可行的是(填字母,后同).
A.加热
B.加KOH固体
C.加水
D.加CH3COONa固体
E.加锌粒
(6)在稀释过程中,随着醋酸浓度的降低,下列各量始终保持增大趋势的是 .
A.C(H+)
B.H+物质的量
C.C(OH﹣)
D.![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:

某化学兴趣小组同学模拟该流程设计了如下实验装置:

回答下列问题:
(1)a处可用来检验I中的反应是否发生,选用的试剂是______________,若要停止I中的化学反应,除停止加热外,还要采取的操作是________________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O ②可能是CuO;③可能是CuS;④_______。乙同学提出假设①一定不成立,该同学的依据是______;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为__________________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________。
(4)为检验制得的硫代硫酸钠产品的纯度,该小组称取5.0g产品配成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:向锥形瓶中加入25.00mL 0.01mol·L-1的KIO3溶液,再加入过量的KI溶液并酸化,发生反应的离子方程式为___________,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应I2 + 2S2O32- == 2I- + S4O62-,当达到滴定终点时,消耗Na2S2O3溶液20.00mL,则该产品的纯度是____________(保留3个有效数字)。
(5)丁同学提出上述实验装置的设计存在不足,建议在I上__________;在I、II之间增加_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com