
����Ŀ���й�����ֵ�������ʾ��2013��ȫ��ƽ����������Ϊ52����֮�����γ���������Ҫ�ɷ�Ϊ�������������ŷŵķ���������β�����ﳾ�ȡ�
��1����֪��CO��g��+H2O��g��![]() CO2��g��+H2��g����H=-4lkJ/mol��ij�¶��£����ݻ�Ϊ2L���ܱ������г���2��0molCO��g����2��0mol H2O��g������tminʱ�ﵽƽ�⣬��÷ų���32��8kJ��������tmin����H2��ʾ��ƽ����Ӧ����Ϊ_________���ɴ˿�֪�ڸ��¶��·�ӦCO��g��+H2O��g��
CO2��g��+H2��g����H=-4lkJ/mol��ij�¶��£����ݻ�Ϊ2L���ܱ������г���2��0molCO��g����2��0mol H2O��g������tminʱ�ﵽƽ�⣬��÷ų���32��8kJ��������tmin����H2��ʾ��ƽ����Ӧ����Ϊ_________���ɴ˿�֪�ڸ��¶��·�ӦCO��g��+H2O��g��![]() CO2��g��+H2��g���Ļ�ѧƽ�ⳣ��Ϊ_________������С�����һλ����
CO2��g��+H2��g���Ļ�ѧƽ�ⳣ��Ϊ_________������С�����һλ����
��2����ʽ��������������������Ҫ����������
����Al2��SO4��3��Һ��Ͷ���ĩ״ʯ��ʯ�����ɼ�ʽ������[Al2��SO4��3Al2O3]��Һ��
����ʽ����������SO2��Al2��SO4��3Al2O3+3SO2=Al2��SO4��3Al2��SO3��3����д��Al2��SO4��3Al2O3������ռ���Һ��Ӧ�Ļ�ѧ����ʽ��_________��
����Al2��SO4��3Al2 ��SO3��3������Al2��SO4��3����ѡ��������Ϊ_________�����������
a��Ũ���� b��KMnO4��Һ C��5%��H2O2��Һ d������
�ò���Ӧ��Ŀ����_________��
���𰸡�
��1��![]() molL-1min-1��
molL-1min-1��![]() ��
��
��2����Al2��SO4��3Al2O3+3H2O+10NaOH=4Na[Al��OH��4]+3Na2SO4��
��cd������Al2��SO4��3ѭ��ʹ��
��������
�����������1����Ӧ�ﵽƽ��ʱ��n��CO��=1mol��![]() =0��8mol���ɴ˿���ø���ֵ�����������ʾ��
=0��8mol���ɴ˿���ø���ֵ�����������ʾ��
CO��g��+ H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼ�� 2mol 2mol 0 0
�仯�� 0��8mol 0��8mol 0��8mol 0��8mol
ƽ���� 1��2mol 1��2mol 0��8mol 0��8mol
ƽ��Ũ����0��6mol/L 0��6mol/L 0��4mol/L 0��4mol/L
����v��H2��=![]() =
=![]() =
=![]() molL-1min-1���˷�Ӧ��ƽ�ⳣ��K1=
molL-1min-1���˷�Ӧ��ƽ�ⳣ��K1=![]() =
=![]() =
=![]() �� �ʴ�Ϊ��
�� �ʴ�Ϊ��![]() molL-1min-1��
molL-1min-1��![]() ��
��
��2��������Al3+��Al2O3�ֱ������������������Һ��Ӧʱ����Na[Al��OH��4]����������Al2��SO4��3Al2O3���ռ���Һ��Ӧ�IJ���ΪNa[Al��OH��4]�Լ�Na2SO4���ɴ˲���д��Al2��SO4��3Al2O3+3H2O+10NaOH=4Na[Al��OH��4]+3Na2SO4���ʴ�Ϊ��Al2��SO4��3Al2O3+3H2O+10NaOH=4Na[Al��OH��4]+3Na2SO4��
��a��Ũ�������������������ӣ���a����ѡ��b


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaOH��KOH�ȼ�����Һ�������������������Լ�ƿ�У���
A. ���в�������ϸ��ƿ B. ���в������Ĺ��ƿ
C. ���ιܵĵ�ƿ D. ����������ϸ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º����£���2mol����A��2mol����Bͨ�����Ϊ2L���ܱ������У��������·�Ӧ��2A(g)+B(g)![]() xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
��1���ӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ ��
��2��x= ��
��3��A��ת������B��ת����֮��Ϊ ��
��4�����и������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־�� ������ĸ����
A��ѹǿ�����仯
B�������ܶȲ����仯
C������ƽ����Է����������ٱ仯
D��A������������B����������֮��Ϊ2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������������������������������������ǣ�
A. OH- B. Mg2+ C. OD- D. D3O+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ͭ�Ʊ�CuSO 4 ��Һ�ж��ַ�����ijʵ��С��������������ַ�����
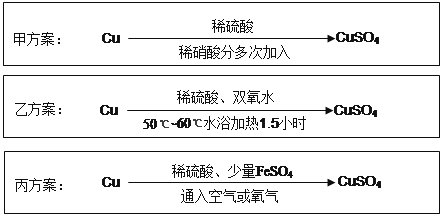
��ش��й����⣺
��1��������
��д���÷�Ӧ�����ӷ���ʽ ��
��Ϊ�˽�Լԭ�ϣ��������������ʵ���֮�����Ϊ��n(H 2 SO 4 )��n(HNO 3 )= ��
��2���ҷ�������6.4gͭ˿�ŵ�90mL 1.5mol��L -1 ��ϡ�����У�������50��������40mL 10%��H2O2����Ӧ0.5Сʱ�����µ�60����������Ӧ1Сʱ��һϵ�в�������CuSO 4��5H 2O 20.0g����֪�й�Ħ��������M(Cu)=64g/mol�� M(CuSO4��5H 2 O) =250g/mol����
����Ӧʱ�¶ȿ�����50��~60�������˹��ߵ�ԭ���� ��
����ʵ��CuSO4��5H 2 O�IJ���Ϊ ��
��3����������������������ֱ��ͨ�뵽ͭ����ϡ����Ļ�����У������ڳ����¼�������Ӧ����ӦҺ�м�����FeSO 4 ����������Ӧ����������ͭ����Ӧ��ȫ������A����pH��4 ��Ȼ����ˡ�Ũ�����ᾧ��
������A��ѡ�����µ� ������ţ���
A��CaO
B��NaOH
C��CuCO 3
D��Cu 2(OH)2CO 3
E��Fe2(SO4) 3
����Ӧ�м�������FeSO 4 �ɼ���ͭ��������FeSO 4 �������� ��
��Ӧ�����еĵ����ӷ���ʽΪ�� ��
��4���Աȼס��ҡ�������ʵ�鷽�������������ŵ��У�д�������� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���в�ҩ��Ƥ�к��е���Ҷ��������ÿ���۵��ʾһ��̼ԭ�ӣ���ԭ��δ�����������п������á���1 mol��Ҷ�������ֱ���Ũ��ˮ��NaOH��Һ��ȫ��Ӧ�������ĵ�Br2��NaOH�����ʵ����ֱ�Ϊ�� ��
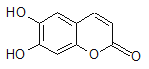
A��2 mol Br2 2 mol NaOH
B��2 mol Br2 3 mol NaOH
C��3 mol Br2 4 mol NaOH
D��4 mol Br2 4 mol NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͪ�������п��������ԣ�6���ǻ���ͪ������ĺϳ�·�����£�
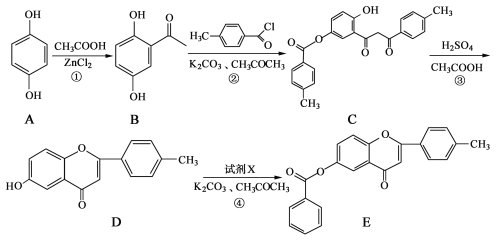
��ش��������⣺
��1��������B�еĺ���������Ϊ �� �������ƣ���
��2����Ӧ�����漰���ķ�Ӧ������ˮ�ⷴӦ�� �� ��
��3����Ӧ���м�����Լ�X�ķ���ʽΪC7H5OCl��X�Ľṹ��ʽΪ ��
��4��B��һ��ͬ���칹����������������
�����ܷ���������Ӧ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��
������������4�ֲ�ͬ��ѧ�������⡣
д����ͬ���칹��Ľṹ��ʽ�� ��
��5����֪�� ����������֪ʶ����������Ϣ��д����
����������֪ʶ����������Ϣ��д����![]() ��CH3COOHΪԭ���Ʊ�
��CH3COOHΪԭ���Ʊ�![]() �ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�
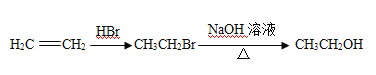
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̬����ɵĻ������0.1mol����ȫȼ�յ�0.15mol CO2��3.6g H2O�����й��ڸû�������˵����ȷ���ǣ� ��
A��һ������ϩ B��һ��û����ϩ C��һ���м��� D������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��D��E��FΪԭ������������������ֶ���������Ԫ�أ��ǽ���Ԫ��A����������������������ͬ��B����������������������������2����B������D�����г��ȼ������������ۻ�����BD2��E+��D2��������ͬ�ĵ�������A������F������ȼ�գ���������ˮ�õ�һ��ǿ�ᡣ����Ӧ����ѧ�����ش��������⣺
��1��A�����ڱ��е�λ���� ��AFD�ĵ���ʽΪ ��
��2��BD2�ĽṹʽΪ �� BD2�γɾ��������Ϊ ��
��3��Ԫ��D��E ��F�γɵļ����ӵİ뾶�ɴ�СΪ �������ӷ��ű�ʾ����
��4��д��ʵ�����Ʊ�����F�����ӷ���ʽ ��
��5��д��E��D�γɵļȺ����Ӽ��ֺ����ۼ��Ļ�������ˮ��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com