
| A. | n=m+1 | B. | n=m+10 | C. | n=m+11 | D. | n=m+25 |
分析 同周期的ⅡA族元素、ⅢA族元素若在短周期为相邻;在四、五周期,中间有10个纵行;在五、六周期应注意存在镧系和锕系,以此来解答.
解答 解:A.若为短周期,ⅡA族元素、ⅢA族元素的原子序数相差1,则n=m+1,故A正确;
B.无论元素在短周期还是长周期,都不存在n=m+10,故B错误;
C.若元素在四、五周期,中间有10个纵行,ⅡA族元素、ⅢA族元素的原子序数相差11,即n=m+11,故C正确;
D.若元素在五、六周期,中间有10个纵行,且存在镧系(14种元素)和锕系,ⅡA族元素、ⅢA族元素的原子序数相差25,即n=m+25,故D正确;
故选B.
点评 本题考查元素周期表及应用,为高频考点,把握元素周期表的结构及族的位置为解答的关键,侧重原子序数关系的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1 | 2 | 3 | 4 | 5 | … | … |
| CH4 | C2H6 | C5H12 | C8H18 | … | … | … |
| A. | C14H30 | B. | C17H36 | C. | C22H42 | D. | C26H54 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
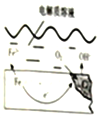 如图是钢铁在潮湿空气能发生电化学腐蚀原理示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈
如图是钢铁在潮湿空气能发生电化学腐蚀原理示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈查看答案和解析>>
科目:高中化学 来源: 题型:选择题
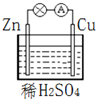
| A. | 该装置能将电能转化为化学能 | B. | 电子由锌片通过导线流向铜片 | ||
| C. | 负极反应为 Zn-2e-═Zn2+ | D. | Cu为正极材料,正极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu与浓硝酸反应:Cu+4H++4NO3-═Cu2++4NO2↑+2H2O | |
| B. | 氨水与醋酸溶液反应:NH3•H2O+CH3COOH═NH4++CH3COO-+H2O | |
| C. | 过氧化钠溶于水:2O2-+2H2O═4OH-+O2↑ | |
| D. | 小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,写出水分子的电子式
,写出水分子的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、氨气和碳酸钠都是电解质 | |
| B. | 常温常压下,22.4L CO2气体的物质的量大于1mol | |
| C. | 2.4克石墨和C60的混合物所含碳原子数约为0.2×6.02×1023 | |
| D. | 氢氧化铁胶体较稳定,是因为该胶体带有正电荷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com