
| A.用酚酞作指示剂时滴定的总反应为:Na2CO3+HCl=NaHCO3+NaCl |
| B.用甲基橙作指示剂时滴定的总反应为:Na2CO3+2HCl=NaCl+CO2↑+H2O |
| C.可用碱式滴定管量取所需要的Na2CO3溶液 |
| D.若酸式滴定管没有用标准溶液润洗,则所测得的碳酸钠溶液浓度偏低 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.c(OH¯)=1×10¯10mol·L¯1 |
| B.c(NH4+)>c(Cl¯)>c(H+)>c(OH¯) |
| C.c(NH3·H2O)=c(NH4+) |
| D.c(H+)+c(NH4+)=c(Cl¯)+ c(OH¯) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
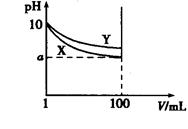
| A.X、Y两种碱溶液中溶质的物质的量浓度一定相等 |
| B.稀释后,X溶液的碱性比Y溶液的碱性强 |
| C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积Vx>Vy |
| D.若8<a<10,则X、Y都是弱碱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
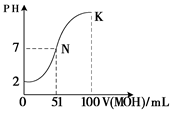
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
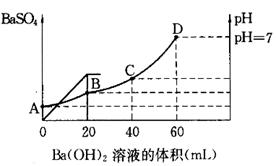
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.01 mol·L-1 | B.0.017 mol·L-1 | C.0.05 mol·L-1 | D.0.50 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 、Cl-四种离子,且c(NH
、Cl-四种离子,且c(NH )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com