
用铂电极电解100mLHNO3与AgNO3的混合液,通电一段时间后,两极均收集到2.24L气体(标况),则原混合液中Ag+的物质的量浓度为
A.1mol/L B.2mol/L C.2.5mol/L D.3mol/L
科目:高中化学 来源:2015-2016学年安徽师大附属中学高一上期中测试化学试卷(解析版) 题型:选择题
某碳酸钠样品中含有碳酸钾,硝酸钠和硝酸钡三种杂质中的一种或两种。现将11g样品加入足量水中,样品全部溶解。再加入过量的氯化钙溶液,得到10g沉淀。对样品所含杂质的正确判断是
A.肯定有硝酸钠
B.肯定有硝酸钠,可能还含有碳酸钾
C.肯定没有硝酸钡,可能有硝酸钠
D.肯定没有碳酸钾和硝酸钡
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上期中测试化学试卷(解析版) 题型:填空题
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、KCl 等混合组成,为了检验它们所含的物质,做了以下实验。
①将固体溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解。
(1)试判断:固体混合物中肯定含有____________,肯定没有_____________________,可能含有________________。
(2)对可能有的物质, 可采用___________ 来检验, 如果含有该物质, 其现象是__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上期中测试化学试卷(解析版) 题型:选择题
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上期中测试化学试卷(解析版) 题型:填空题
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
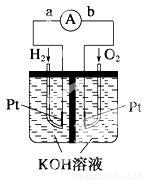
(1)氢氧燃料电池的能量转化主要形式是______________________,在导线中电子流动方向为_______(用a、b 表示)。
(2)负极反应式为 ___________________。
(3)电极表面镀铂粉的原因为___________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ.2Li+H2 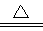 2LiH
2LiH
Ⅱ.LiH+H2O═LiOH+H2↑
①反应Ⅰ中的还原剂是______________,反应Ⅱ中的氧化剂是_____________。
②用锂吸收224L(标准状况)H2,再由生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上期中测试化学试卷(解析版) 题型:选择题
下列各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是

A.②>①>③>④ B.④>②>①>③ C.④>②>③>① D.③>②>④>①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上期中测试化学试卷(解析版) 题型:填空题
按要求填写下列空格
①0.5molH2O约含______个质子;
②1.204×1024个水分子的质量为________g;
③5mol的CO2与8mol的SO2原子数比是_________;
④写出属于氧化还原反应但不属于化合反应、分解反应、置换反应和复分解反应的反应式一例:__________。
⑤写出Na3PO4在水溶液中的电离方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃天水一中高一上第二学段段中测化学卷(解析版) 题型:填空题
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示。(已知:NH4++OH- NH3↑+H2O)
NH3↑+H2O)
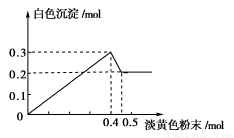
根据题意回答下列问题:
(1)淡黄色粉末为____________(填名称)。
(2)溶液中肯定有______________离子,肯定没有__________离子。
(3)溶液中离子的物质的量之比为______________________________。
(4)写出沉淀部分减少时的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上期中测试化学试卷(解析版) 题型:填空题
(1)实验测得,8g甲烷在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113kJ的热量,试写出甲烷燃烧的热化学方程式_________________________
(2)在压强为0.1MPa条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发反应生成甲醇:
CO(g)+2H2(g) CH30H(g)
CH30H(g)
①该反应的△H_____0,___0(填“>”、“<”或“=”)
②若容器容积不变,下列措施可增加甲醇产率的是____________
A.升高温度
B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大
D.再充人lmolCO和3mol H2
(3)以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.0kJ•mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g)△H=-129.0kJ•mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com