
煤气化过程中生成的CO和H2一定条件下制甲醇的反应如下:
CO(g)+ 2H2(g) CH3OH(g) △H < 0。其他条件不变,改变某一条件后,用示意图表示的反应变化正确的是
CH3OH(g) △H < 0。其他条件不变,改变某一条件后,用示意图表示的反应变化正确的是
A | B | C | D | |
改变的条件 | 压强 | 温度 | 平衡体系增加H2 | 催化剂 |
变化的示意图 |
|
|
|
|
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年福建省漳州市八校高三3月联考理综化学试卷(解析版) 题型:选择题
化学与社会、生产、生活紧切相关,下列说法正确的是
A.信息产业中的光缆的主要成份是单质硅
B.NO2、CO2、SO2、PM2.5颗粒都会导致酸雨
C.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强
D.发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
常温下向盛水烧杯中加2g生石灰(如下图)。搅拌后再恢复到原温,在此过程中,下列说法正确的是
A.水的电离常数不变
B.Ca(OH)2 的电离程度先大后变小然最后不变
C.水的电离平衡向逆反应方向移动最后不变
D.水的电离度将会先变小然后变大最后不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
化学学科需要借助化学专用语言描述,下列有关化学用语正确的是
A.CO2分子比例模型:
B.NH4I的电子式:
C.乙醇的结构简式:C2H5OH
D.K+最外层电子排布式:4S24P6
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
25℃时,0.1 mol/L 的CH3COOH溶液 pH =3,0.1 mol/L的HCN溶液pH=4。下列说法正确的是
A.CH3COOH与HCN均为弱酸,酸性:HCN > CH3COOH
B.25℃时,水电离出来的c(H+)均为 10-11mol/L的两种酸,酸的浓度:HCN > CH3COOH
C.25℃时,浓度均为0.1 mol/L 的CH3COONa和NaCN溶液中,pH大小:CH3COONa >NaCN
D.25℃时,pH均为3的CH3COOH与HCN溶液各100ml与等浓度的NaOH溶液反应,消耗NaOH溶液体积:CH3COOH >HCN
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
下列比较中不正确的是
A.金属性:K > Na > Li
B.热稳定性:HI > HCl > HF
C.非金属性:F > O > N
D.碱性:NaOH > Mg(OH)2 > Al(OH)3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:填空题
(12分)镁铝碱式碳酸盐[MgaAlb(OH)c(CO3)d·x H2O]阻燃剂具有阻燃、消烟、填充等功能,是一种不溶于水的新型无机阻燃剂。
(1)将MgaAlb(OH)c(CO3)d·x H2O表示成氧化物形式 。
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:
准确称取15.050 g样品进行灼烧至恒重,生成CO2 0.560 L(已换算成标准状况下)。分析测得残留物中MgO为6.000 g,Al2O3为2.550 g,通过计算确定该镁铝碱式碳酸盐的化学式。(写出计算过程)
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是
A.使用可降解塑料聚二氧化碳,能减少白色污染
B.实施“煤改气”、“煤改电”等清洁燃料改造工程,有利于保护环境
C.雷雨过后感觉到空气清新是因为空气中产生了少量的二氧化氮
D.通常所说的三大有机合成材料是指塑料、合成纤维、合成橡胶
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期二模考试理综化学试卷(解析版) 题型:简答题
(14分)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.
I.已知:2CO(g)+ O2(g)=2CO2(g),ΔH=-566 kJ·mol-1
2Fe(s)+ 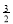 O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
反应:Fe2O3(s)+ 3CO(g)  2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
Ⅱ.反应  Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g) 
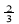 Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡.
Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡.
(1)CO的平衡转化率=____________.
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________.
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:
CO(g)+ 2H2(g)  CH3OH(g).请根据图示回答下列问题:
CH3OH(g).请根据图示回答下列问题:
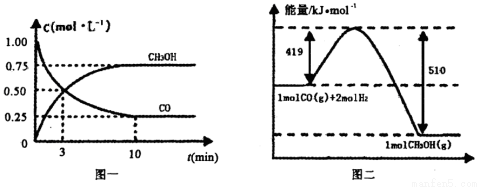
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________.
(2)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1 kJ热量 |
乙 | 1mol CH3OH | α2 | c2 | 吸收Q2 kJ热量 |
丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3 kJ热量 |
则下列关系正确的是________.
A.c1=c2
B.2Q1=Q3
C.2α1=α2
D.α1+α2 =1
E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量
(3)若在一体积可变的密闭容器中充入l mol CO、2mol H2和1mol CH3OH ,达到平衡吋测得混合气体的密度是同温同压下起始的1.6倍,则该反应向______(填“正”、“逆”)反应方向移动.
(4)甲醇可与氧气构成燃料电池,该电池用多孔的惰性电极浸入浓氢氧化钾溶液,写出该电池的负极反应式__________________ ____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com