
向含2 mol NaOH、1 mol Ba(OH)2、2 mol Na[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量的关系不正确的是( )
选项 | A | B | C | D |
n(CO2)(mol) | 2 | 3 | 4 | 6 |
n(沉淀)(mol) | 1 | 2 | 3 | 2 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| B. | 32g甲醇中存在的共价键总数是6 NA | |
| C. | 1L 0.1mol•L-1的NaHCO3溶液中氧原子数为0.3NA | |
| D. | 235g核素92235U中的中子数为92 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量NaHCO3溶液与Ca(OH)2溶液反应:OH-+HCO3-=CO32-+H2O | |
| B. | 向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH)3↓ | |
| C. | 实验室用NH4Cl和Ca(OH)2共热制取NH3:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | CO2和足量澄清石灰水反应:CO2+Ca2++2OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7gCnH2n中含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCHCl3中含原子总数等于5NA | |
| C. | 1molC5H12分子中所含单键数为15NA | |
| D. | 标准状况下,11.2L已烷中含3mol碳原子 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:推断题
某无色溶液中含有K+、Cl-、OH-、SO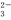 、SO
、SO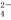 ,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
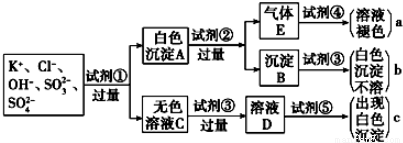
(1)图中试剂①~⑤溶质的化学式分别是
①________,②________,③________,④__________,⑤__________。
(2)图中现象a、b、c表明检验出的离子分别是a________、b________、c________。
(3)白色沉淀A加试剂②反应的离子方程式_________________。
(4)无色溶液C加试剂③的主要目的 是_____________________。
是_____________________。
(5)白色沉淀 A若加试剂③而不加试剂②,对实验的影响是____________________。
A若加试剂③而不加试剂②,对实验的影响是____________________。
(6)气体E通入试剂④发生反应的离子方程式是____________________。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
下列各组物质按右图所示转化关系每一步都能一步实现的是
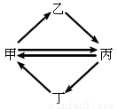
甲 | 乙 | 丙 | 丁 | |
A. | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 |
B. | NO | HNO3 | NO2 | NH3 |
C. | Cu | CuO | CuSO4 | CuCl2 |
D. | Si | Na2SiO3 | SiO2 | SiF4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
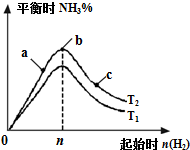 某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):
某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com