
| A�� | ��APEC������2014���µ�����ʻ㣬����2014��APEC�����ڼ䱱����������գ�˵������ʵʩ��·���к���Ⱦ��ҵͣ���ȴ�ʩ���Լ�����������֤������������Ч�� | |
| B�� | ���ع��͡������ӹ��������������Ʒ������������ | |
| C�� | ��ʯ�ҡ����ۡ��轺��ʳƷ��װ�г��õĸ���� | |
| D�� | ����������������� |
���� A����·���пɼ�������β���ŷţ���Ⱦ��ҵͣ���ɼ�����Ⱦ��
B�������ع��͡��Ƴɷ��������Ա��Ϊ����
C�������ǿ���������
D��������Ҫ�ɷ��Ǽ��飬���л����������������£���������ķ������ö����ɵ�һ�ֻ�����壮
��� �⣺A����·���пɼ�������β���ŷţ���Ⱦ��ҵͣ���ɼ�����Ⱦ���ɼ�����������֤������������A��ȷ��
B�����ع��͡�����һ������������������ķ�ʳ���ͣ������Ƴɷ�����ʵ����ʹ������֬��������Ӧ������ʳ���ͱ�ɷ��������������Դ�������ʣ���B��ȷ��
C�������ǿ������������Ǹ��������C����
D��������Ҫ�ɷ��Ǽ��飬���л����������������£���������ķ������ö����ɵ�һ�ֻ�����壬��D��ȷ��
��ѡC��
���� ���⿼���˳���ʳƷ���Ӽ����ع��͵������г��������ʵ����ʣ���Ϥ���ʵ������ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
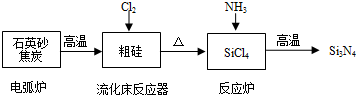
| ���� | Si | SiCl4 | Cl2 |
| �е�/�� | 2355 | 57.6 | -34.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ����MgCl2��AlCl3�����Һ�У���ʼ�μ�6ml�Լ�A��֮��ĵ��Լ�B�����ó���y mol���Լ����V��ml����Ĺ�ϵ�����½��۲���ȷ���ǣ�������
��ͼ����MgCl2��AlCl3�����Һ�У���ʼ�μ�6ml�Լ�A��֮��ĵ��Լ�B�����ó���y mol���Լ����V��ml����Ĺ�ϵ�����½��۲���ȷ���ǣ�������| A�� | A��NaOH��B�����ᣬ��C��NaOH����C��HCl��=2��1 | |
| B�� | ԭ���Һ�У�C��Al3+����C��Mg2+����C��Cl-��=1��1��5 | |
| C�� | A��NaOH��B�����ᣬ��C��NaOH����C��HCl��=1��2 | |
| D�� | ��6��9����Ӧ���ӷ�ӦʽH++OH-=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ���������ԭ�Ӱ뾶Խ���۵�Խ�� | |
| B�� | ���Ӽ�������Խǿ�����Ӿ�����۵�Խ�� | |
| C�� | ϡ������ԭ������Խ���۵�Խ�� | |
| D�� | ͬ����Ԫ�ص�ԭ�Ӱ뾶ԽС��Խ��ʧȥ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | |
| Ũ��1 | 0.05mol•L-1 | amol•L-1 | 0.05mol•L-1 |
| Ũ��2 | 0.078mol•L-1 | 0.078mol•L-1 | 0.122mol•L-1 |
| Ũ��3 | 0.06mol•L-1 | 0.06mol•L-1 | 0.04mol•L-1 |
| Ũ��4 | 0.07mol•L-1 | 0.07mol•L-1 | 0.098mol•L-1 |
| A�� | ��[Ũ��3]��[Ũ��1]�ıȽϣ����жϳ�����Ӧ�Ƿ��ȷ�Ӧ | |
| B�� | ��[Ũ��2]��[Ũ��1]�ıȽϣ����ж�ƽ���ƶ���ԭ���������¶� | |
| C�� | [Ũ��1]��a=0.05mol•L-1 | |
| D�� | ����ijѧ����ʵ��ٹ����У���ø�������ijһʱ�̵�Ũ��Ϊ[Ũ��4]����[Ũ��1]�Ƚϣ��ɷ��ָ�ͬѧ�ڲⶨ[Ũ��4]��������ʱ�����˺ܴ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡHNO3�еμ�Na2SO3��Һ��SO32-+2H+=SO2��+H2O | |
| B�� | ����������Һ�м����������ữ�Ĺ���������Һ Fe2++2H++H2O2�TFe3++2H2O | |
| C�� | Mg��HCO3��2��Һ�м������ʯ��ˮ��Mg2++2HCO3-+Ca2++2OH-=CaCO3��+2H2O+MgCO3�� | |
| D�� | �� 0.5 mol��FeBr2��Һ��ͨ��13.44L����״���£�Cl2��10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com