解:(1)燃烧黄铁矿反应,反应物为FeS
2和O
2,生成物为Fe
2O
3和SO
2,根据化合价升降法配平,
FeS
2+O
2--Fe
2O
3+SO
2 ,FeS
2中Fe为+2价,S为-1价,O
2中O为0价,Fe
2O
3中Fe为+3价、O为-2价,SO
2中S为+4价、O为-2价,
FeS
2中:铁元素上升1价,硫元素上升5价×2,则总共上升11价,
O
2中:氧元素降低2价×2,则总共降低4价.所以FeS
2前计量数为4,O
2前计量数为11,再根据原子守恒,配出Fe
2O
3前计量数为2,SO
2前计量数为8,
则方程式为4FeS
2+11O
2
2Fe
2O
3+8SO
2,故答案为:4FeS
2+11O
2
2Fe
2O
3+8SO
2;
(2)接触室中发生的反应是二氧化硫的催化氧化,产物为三氧化硫,然后配平即得方程式,为2SO
2+O
2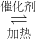
2SO
3,故答案为:2SO
2+O
2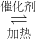
2SO
3;
(3)a、在沸腾炉中,原料黄铁矿是固体、空气是气体,为了加快反应速率,所以要将黄铁矿粉碎,增大接触面,提高反应速率,故a正确;
b、转化率=已转化的原料的量/原料的总量×100%,接触室中反应2SO
2+O
2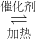
2SO
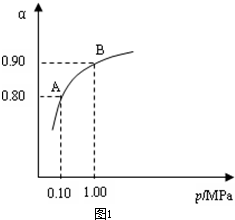
3,为可逆反应,采用空气过量目的是增大氧气浓度,促使平衡正向移动,导致SO
2更多的转化成SO
3,所以SO
2转化率提高,故b正确;
c、催化剂只能改变反应速率,不能影响转化率,故c不正确;
d、沸腾炉排出的矿渣中主要成分为Fe
2O
3,可作为炼铁原料,故d正确;
故答案为:abd;
(4)吸收塔中SO
3如果用水吸收,发生反应:SO
3+H
2O═H
2SO
4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,
故答案为:避免形成酸雾;
(5)方法①:先用氨水吸收时,发生反应:SO
2+2NH
3?H
2O═(NH
4)
2SO
3,再用浓硫酸处理时,发生反应:
(NH
4)
2SO
3+H
2SO
4═(NH
4)
2SO
4+SO
2↑+H
2O,故可获得较高浓度的SO
2,
方法②:先用含一定水的亚硫酸钠吸收,发生反应:Na
2SO
3+SO
2═2NaHSO
3;后再加热处理时,发生反应:
2NaHSO
3
Na
2SO
3+SO
2↑,故也可获得较高浓度的SO
2,同时亚硫酸钠又可再次用于吸收SO
2,循环利用,而所需能量可由流程中三步骤放热反应产生的废热提供,
故答案为:获得较高浓度的SO
2;流程中三步骤产生的废热提供;亚硫酸钠可以循环利用;
(6)SO
2具有还原性,可与多种氧化剂反应,如O
2、H
2O
2、Na
2O
2、酸性KMnO
4溶液、氯水、溴水、碘水等,
根据题意,工业制溴过程中用SO
2吸收潮湿空气中的Br
2,可确定反应物为SO
2、Br
2、H
2O,在反应过程中SO
2表现还原性,
其中+4价硫化合价上升到+6价,生成H
2SO
4,Br
2表现氧化性,化合价降低到-1价,生成HBr.配平得化学方程式为SO
2+Br
2+2H
2O=2HBr+H
2SO
4,SO
2是气体、Br
2是单质、H
2O是弱电解质都必须保留化学式,HBr和H
2SO
4都是强酸,易溶于水、易电离,所以要改写成离子形式,
即HBr═H
++Br、H
2SO
4═2H
++SO
42-,则得离子方程式SO
2+Br
2+2H
2O=4H
++2Br
-+SO
42-,
故答案为:SO
2+Br
2+2H
2O=4H
++2Br
-+SO
42-.
分析:(1)燃烧黄铁矿反应生成氧化铁和二氧化硫,再根据化合价升降法配平方程式;
(2)接触室中发生二氧化硫的催化氧化反应,产物为三氧化硫,最后配平方程式.注意反应条件;
(3)第一步:SO
2的制取.主要原料是黄铁矿和空气,在高温下煅烧,使硫元素转变成SO
2气体,反应方程式为
4FeS
2+11O
2
2Fe
2O
3+8SO
2,设备为沸腾炉.黄铁矿需要粉碎,以增大和空气的接触面;
第二步:SO
3的制取.从沸腾炉中出来的气体需经过净化、除尘,进入接触室在催化剂作用下SO
2和O
2反应生成SO
3,设备为接触室.同时涉及热量的交换、催化剂的作用、平衡的移动等问题;
第三步:硫酸的生成.从接触室中出来的气体进入吸收塔,为避免酸雾形成需用浓H
2SO
4吸收;
(4)吸收塔中吸收三氧化硫气体的吸收液的选择及原因;
(5)两种尾气处理方法的原理、优缺点;
(6)SO
2具有还原性,可与多种氧化剂反应,如O
2、H
2O
2、Na
2O
2、酸性KMnO
4溶液、氯水、溴水、碘水等.确定出反应物与生成物后,再配平,最后改写成离子方程式.
点评:本题考查工业接触法制硫酸的原理,同时涉及到反应速率、转化率、反应的热效应、工业尾气的处理等内容,具有一定的综合性,需要一定的知识迁移能力,难度中等.化学方程式的反应条件容易忽略.

 2Fe2O3+8SO2,故答案为:4FeS2+11O2
2Fe2O3+8SO2,故答案为:4FeS2+11O2 2Fe2O3+8SO2;
2Fe2O3+8SO2;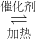 2SO3,故答案为:2SO2+O2
2SO3,故答案为:2SO2+O2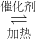 2SO3;
2SO3; 2SO3,为可逆反应,采用空气过量目的是增大氧气浓度,促使平衡正向移动,导致SO2更多的转化成SO3,所以SO2转化率提高,故b正确;
2SO3,为可逆反应,采用空气过量目的是增大氧气浓度,促使平衡正向移动,导致SO2更多的转化成SO3,所以SO2转化率提高,故b正确; Na2SO3+SO2↑,故也可获得较高浓度的SO2,同时亚硫酸钠又可再次用于吸收SO2,循环利用,而所需能量可由流程中三步骤放热反应产生的废热提供,
Na2SO3+SO2↑,故也可获得较高浓度的SO2,同时亚硫酸钠又可再次用于吸收SO2,循环利用,而所需能量可由流程中三步骤放热反应产生的废热提供, 2Fe2O3+8SO2,设备为沸腾炉.黄铁矿需要粉碎,以增大和空气的接触面;
2Fe2O3+8SO2,设备为沸腾炉.黄铁矿需要粉碎,以增大和空气的接触面;


 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题: