
用1.0 mol.L-l NaOH溶液中和某浓度H2 SO4溶液时,其pH和所加NaOH溶液的体积(V)关系如图所示。则原硫酸溶液的物质的量浓度和恰好中和时溶液的总体积分别是(假设混合后溶液总体积为二者体积之和)( )
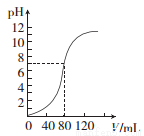
A.0.5 mol·L-1、160 mL B.1.0 mol·L-1、160 mL
C.0.5 mol·L-1、80 ml。 D.1.0 mol·L-1、80 ml。
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高二上期中化学卷(解析版) 题型:选择题
常温下,对下列四种溶液的叙述正确的是( )
① | ② | ③ | ④ | |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.四种溶液分别加水稀释10倍,pH变化最大的是①和④
B.②、④两溶液相比,两者的kw相同
C.①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D.①、④两溶液按一定体积比混合,所得溶液中离子浓度顺序一定为:
c(NH4+)>c(Cl-)>c(H+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷(解析版) 题型:选择题
某温度下将Cl。通人KOH溶液里,反应后得到KC1、KC1O、KC1O3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为3:1,则Cl2与KOH反应时,被还原的氯元素和被氧化的氯元素的质量之比为( )
A.1 : 3 B.4 : 3 C.2 : 1 D.3 : 1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高二上学期期中化学试卷(解析版) 题型:填空题
煤和煤制品(如水煤气、焦炭、甲醚等)已广泛应用于工农业生产中。
(1)已知:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3 kJ.mol-l
CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.3 kJ.mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为____________,该反应在_________(填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g) N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:
N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:

①10~20 min内,N2的平均反应速率可v(N2)=____________。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_______(填字母)。
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.遁当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:

若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020 mol.L-l,在该条件下达到平衡时,CO的转化率为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高二上学期期中化学试卷(解析版) 题型:选择题
在一定条件下,将3 mol A和1 mol B两种气体混合于2L恒容密闭容器中,发生如下反应:3A(g) + B(g)  xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
A.A的转化率为40%
B.2 min内B的反应速率为0.2 mol.L-l.min-1
C.x=2
D.若混合气体的密度不变,则表明该反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:计算题
工业电解饱和食盐水产生的氯气制漂白粉,所进行的反应是
① 2NaCl+2H2O Cl2+H2+2NaOH
Cl2+H2+2NaOH
② 2Ca(OH)2(石灰乳)+ 2Cl2 =CaCl2+Ca(ClO)2+2H2O
某厂日产漂白粉(含量80%,主要杂质Ca(OH)2)20吨,已知进行①步反应的转化率90%,进行②步转化率85%。
(1)写出②反应的离子方程式并用双线桥标出电子转移数目
(2)列式计算该厂日消耗精制后的NaCl多少摩尔?(科学计数值,保留小数点后两位)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
某实验室合成了一种可溶的金属氯化物(RClx),为了测定该金属氯化物的成分,研究人员做了以下实验:取物质的量浓度为0.05 mol/L的金属氯化物(RClx)溶液20mL,使之恰好与20 mL 0.15mol/L的AgNO3溶液完全反应.则该氯化物的化学式为
A.RCl B.RC12 C.RC13 D.RCl4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
在下列三个反应中加
①H2O2+H2S=2H2O+S
②2H2O2=2H2O+O2
③H2O2+Cl2=2HCl+O2,
从氧化还原角度分析H2O2所起的作用是
A.①氧化剂 ②还原剂 ③氧化剂 B.①还原剂 ②氧化剂 ③氧化剂
C.①氧化剂②氧化剂③氧化剂 D.①氧化剂 ②既是氧化剂又是还原剂 ③还原剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:实验题
盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常 见的试剂.
见的试剂.
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式 (中和热数值为57.3kJ/mol):
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因可能是 _(填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
(1)某学生用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂.实验中不必用到的是
A.酸式滴定管 B.容量瓶 C.锥形瓶 D.铁架台
(2)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________.当________时,即停止滴定.
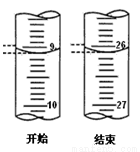
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:已知用c(HCl)=0.10 mol/L的盐酸标定25mL的氢氧化钠溶液,测得c(NaOH)______ ___mol/L
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是___ ___(填序号).
A.锥形瓶用蒸馏水洗净后没有干燥
B.碱式滴定管未用待测液润洗就直接注入待测氢氧化钠溶液
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com