
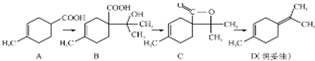
 胡妥油(D)用作香料的原料,它可由A合成得到:
胡妥油(D)用作香料的原料,它可由A合成得到:| A. | 按系统命名法有机物A的名称为3-甲基-3-环已烯甲酸 | |
| B. | 如果条件合适,B可能发生加聚反应,也可能发生缩聚反应 | |
| C. | C 的分子式为C10H14O2 | |
| D. | D 与Br2的CCl4溶液反应,最多有4种生成物 |
分析 A.A中含有甲基和羧基位于对位位置;
B.B含有碳碳双键,可发生加聚反应,含有羟基、羧基,可发生缩聚反应;
C.由结构简式确定;
D.D和溴发生加成反应,最多有3种生成物.
解答 解:A.A中含有甲基和羧基位于对位位置,名称应为1-甲基-4-环已烯甲酸,故A错误;
B.B中含有碳碳双键、羧基和醇羟基,具有烯烃、羧酸和醇的性质,所以B能发生加聚反应、缩聚反应,故B正确;
C.由结构简式可知C 的分子式为C10H16O2,故C错误;
D.D和溴发生加成反应,可能是一个双键发生加成反应、可能是两个双键发生加成反应,所以最多有3种生成物,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、醇性质及同分异构体的考查,选项CD为易错点,题目难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
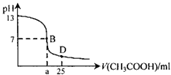 如图为常温下,向25ml某浓度的NaOH溶液中逐滴加入0.2mol•L-1CH3COOH溶液的过程中溶液pH的变化曲线,下列说法不正确的是( )
如图为常温下,向25ml某浓度的NaOH溶液中逐滴加入0.2mol•L-1CH3COOH溶液的过程中溶液pH的变化曲线,下列说法不正确的是( )| A. | NaOH溶液起始浓度为0.1mol•L-1 | |
| B. | a>12.5 | |
| C. | B点溶液中c(Na+)一定等于c(CH3COO-) | |
| D. | D点溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
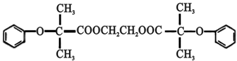 )可由下列路线合成:
)可由下列路线合成: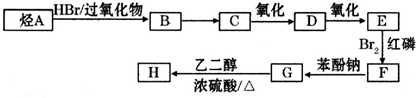
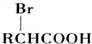
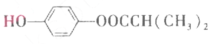 .
.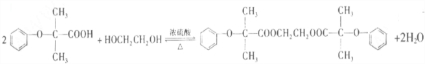 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “地沟油”危害健康,是因为脂肪酸油脂中的碳碳双键被破坏,不利健康 | |
| B. | 浸泡过高锰酸钾溶液的硅藻土可用作水果保鲜制是因为高锰酸钾溶液可吸收水果释放的乙烯 | |
| C. | 废旧电池必须回收利用,是因为电池中的重金属等会严重污染土壤和水体 | |
| D. | 食品包装袋、食物保鲜膜通常用聚乙烯树脂,是因为聚乙烯树脂是无毒的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
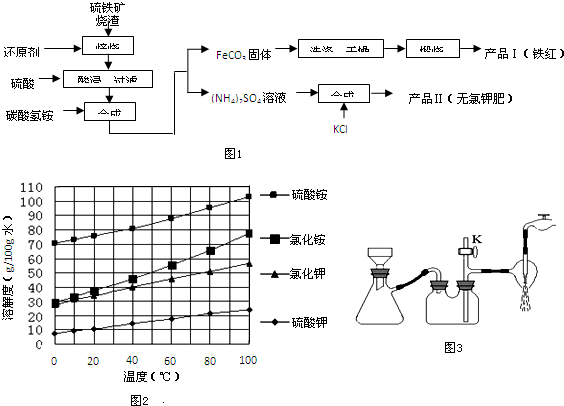
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
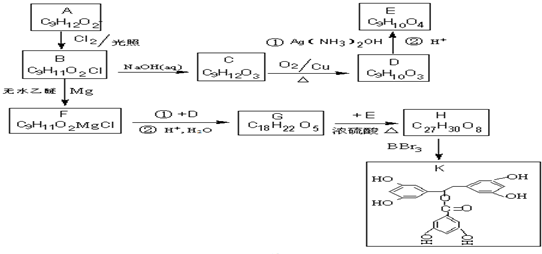
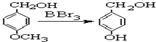
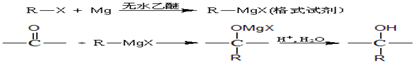
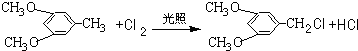 .
.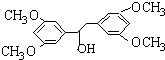 ;
;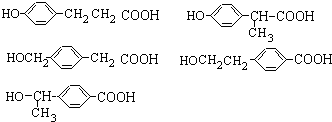 (任意3个);.
(任意3个);.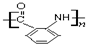 .(无机试剂任选.用流程图表示:写出反应物、产物及主要反应条件).
.(无机试剂任选.用流程图表示:写出反应物、产物及主要反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯通入溴的四氯化碳溶液中,溶液褪色 | |
| B. | 苯滴加到溴水中,振荡后水层接近无色 | |
| C. | 将灼热的铜丝迅速插入乙醇中,反复多次,有刺激性气味产生 | |
| D. | 甲烷和氯气的混合气体在光照后,瓶壁上有油状液滴附着 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
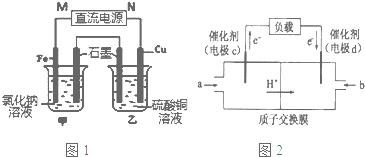
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
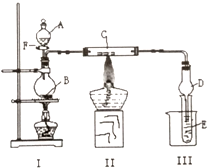 用如图所示装置进行有关实验,拔掉分液漏斗上口玻璃塞,打开F,将A逐滴加入至B中.
用如图所示装置进行有关实验,拔掉分液漏斗上口玻璃塞,打开F,将A逐滴加入至B中.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com