
| A. | 该有机物分子中C、H、O原子个数比为1:2:3 | |
| B. | 该有机物中必定含有氧元素 | |
| C. | 该有机物分子中C、H原子个数比为1:2 | |
| D. | 该有机物化学式为C2H4 |
分析 该有机物生成的水和二氧化碳的物质的量比为1:1,所以可以据此可以求算出其中碳原子和氢原子的个数比,但是不能判断其中氧原子与碳原子及氢原子的个数比,然后结合质量守恒定律即可完成判断.
解答 解:A.有机物在O2中充分燃烧生成CO2和H2O的物质的量之比为1:1,根据质量守恒定律可以判断在有机物中含有碳原子和氢原子,但是不能判断出该有机物中是否含有氧元素,故A错误;
B.有机物是指含碳的化合物,该有机物的质量未给出,无法判断有机物中是否含有氧元素,故B错误;
C.根据题意可以知道生成的水和二氧化碳的物质的量比为1:1,即生成的水和二氧化碳的分子个数相等,而一个水分子中含有2个氢原子,一个二氧化碳分子中含有一个碳原子,即该有机物中碳原子和氢原子的个数比为:1:2,故C正确;
D.根据质量守恒定律可以判断在有机物中含有碳原子和氢原子,但是不能判断出该有机物中是否含有氧元素,则无法确定该有机物的分子式,故D错误;
故选C.
点评 本题考查有机物分子式确定的计算与判断,题目难度中等,注意明确本题中利用原子守恒确定有机物分子中C、H原子个数之比,但不能确定是否含有氧元素.


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:选择题
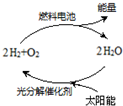 能源是当今社会发展的三大支柱之一.有专家预测氢能源将是未来最理想的新能源,而最理想的氢的循环模式如图,此循环可以节约原料,缓解能源危机.在此构想的物质循环中太阳能最终转化为( )
能源是当今社会发展的三大支柱之一.有专家预测氢能源将是未来最理想的新能源,而最理想的氢的循环模式如图,此循环可以节约原料,缓解能源危机.在此构想的物质循环中太阳能最终转化为( )| A. | 化学能 | B. | 热能 | C. | 生物能 | D. | 电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应为4OH--4e-=2H2O+O2↑ | |
| B. | 放电时CO32-向负极移动 | |
| C. | 电池放电时,电池中CO32-的物质的量将逐渐减少 | |
| D. | 电路中电子由负极、经熔融的K2CO3流到正极,形成闭合回路 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x的原子序数大于y的原子序数 | |
| B. | x的电负性小于y的电负性 | |
| C. | x的离子半径大于y的离子半径 | |
| D. | x的第一电离能小于y 的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
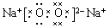 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com