
| A. | SO2 | B. | CaO | C. | CO | D. | NaOH |
分析 由两种元素组成,其中一种元素为氧元素的化合物为氧化物.
碱性氧化物是指能跟酸起反应,生成盐和水的氧化物.一般来说金属氧化物大部分是碱性氧化物,而且碱性氧化物一定是金属氧化物.
能跟碱起反应,生成盐和水的氧化物属于酸性氧化物.
既能和酸反应,又能和碱反应的氧化物属于两性氧化物.
既不能和酸反应,又不能和碱反应的氧化物属于不成盐氧化物.
解答 解:A.二氧化碳为氧化物,能跟碱起反应,生成盐和水,属于酸性氧化物,不能与酸反应,不属于碱性氧化物,故A错误;
B.氧化钙为氧化物,它能和酸反应生成盐和水,如与盐酸反应生成氯化钙和水,是碱性氧化物,故B正确;
C.CO既不能和酸反应,又不能和碱反应,属于不成盐氧化物,故C错误;
D.NaOH由三种元素组成,不属于氧化物,故D错误;
故选B.
点评 本题考查碱性氧化物的判别,抓住碱性氧化物的概念关键词进行解答,注意大多数金属氧化物是碱性氧化物,可以说碱性氧化物一定是金属氧化物,但不能说金属氧化物一定是碱性氧化物,题目较简单.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:解答题
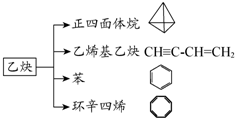 乙炔是一种重要的有机合成原料,以乙炔为原料在不同的反应条件下可以转化成如图所示的各种有机化合物.请回答下列问题:
乙炔是一种重要的有机合成原料,以乙炔为原料在不同的反应条件下可以转化成如图所示的各种有机化合物.请回答下列问题: -CH=CH2、
-CH=CH2、 的反应为取代反应
的反应为取代反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L水中含有1 mol H2SO4 | |
| B. | 1 L溶液中含有1 mol H+ | |
| C. | 将98 g H2SO4溶于1 L水中配成溶液 | |
| D. | 1 L H2SO4溶液中含98 g H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2、Na2O2都属于过氧化物,都存在非极性共价键 | |
| B. | 1mol H2O2在参加反应时可能转移lmol或2mol电子 | |
| C. | H2O2在酶作用下催化分解,随着温度的升高,分解速率持续加快 | |
| D. | H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似、与SO2不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、NO3- | B. | Na+、Cl- | C. | Na+、NO3- | D. | Cl-、Na+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

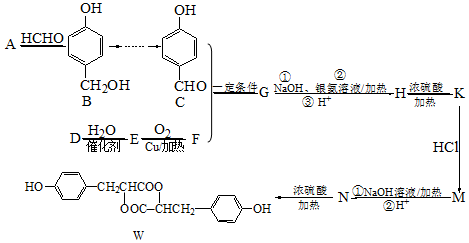
 .
.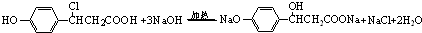 .
.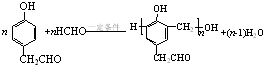 .
.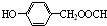 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体 | |
| B. | 除去MgCl2中的Fe3+,可以加入NaOH固体 | |
| C. | 明矾净水的反应:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| D. | 加热蒸干KCl溶液,最后得到KOH固体(不考虑CO2的反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com