
| c(OH-)V碱-c(H+)V酸 |
| V碱+V酸 |
| c(OH-)V碱-c(H+)V酸 |
| V碱+V酸 |
| 0.1×V碱-0.01×V酸 |
| V碱+V酸 |


科目:高中化学 来源: 题型:
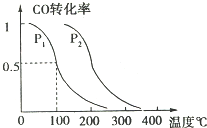 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液氨可用作致冷剂 |
| B、向Fe( OH ) 3 胶体中滴入过量的NaHSO4溶液,能使胶体发生凝聚而沉淀 |
| C、熔融状态下能够导电的化合物中一定存在离子键 |
| D、28g 乙烯和氮气的混合气体中含有NA个原子(戈代表阿伏加德罗常数的值) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2>I2>Fe3+>SO2 |
| B、Cl2>Fe3++>I2>SO2 |
| C、Fe3+>Cl2>I2>SO2 |
| D、Cl2>Fe3+>SO2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16g氧气和臭氧的混合物中含有NA个氧原子,该混合物的体积一定小于11.2 L |
| B、1 L 0.2 mol/L的CH3COOH溶液中,H+数目为0.2NA |
| C、5.6g铁与足量氯气或硫蒸气反应转移的电子数为0.3NA |
| D、在常温常压下,等质量的H2和O2的体积之比是16:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
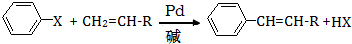 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)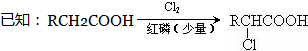
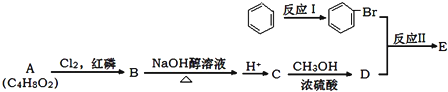
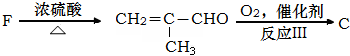
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com